Importantísima revisión de la aplicación de inteligencia artificial en la atención médica. – Gestión y Economía de la Salud

por Vangelis D. Karalis.

El propósito de esta revisión de la literatura es proporcionar una sinopsis fundamental de la investigación actual relacionada con la inteligencia artificial (IA) dentro del ámbito de la práctica clínica.
El realizar este posteo visibilizando un trabajo de revisión con 193 citas bibliográficas es útil para ilustrar donde estamos frente a la inteligencia artificial y sus aplicaciones más desarrolladas en diferentes áreas del campo clínico. Es mucho e importante lo que tienen que aprender los equipos de salud del futuro sobre esto. Revisar, ser críticos, estudiar, volver sobre los pasos, un camino sinuoso, con un norte claro, mejorar la calidad de atención y las seguridad de los pacientes.
La inteligencia artificial Esta revolucionando el campo de la medicina y la atención sanitaria al proporcionar soluciones innovadoras a problemas complejos.
Uno de los beneficios más importantes de la IA en la práctica clínica es su capacidad para investigar grandes volúmenes de datos con eficiencia y precisión. Esto ha llevado al desarrollo de diversas aplicaciones que han mejorado los resultados de los pacientes y han reducido la carga de trabajo de los profesionales sanitarios.
La IA puede ayudar a los médicos a realizar diagnósticos más precisos y desarrollar planes de tratamiento personalizados. Se describen ejemplos exitosos de aplicaciones de IA para una serie de especialidades médicas como cardiología, cirugía, gastroenterología, neumología, nefrología, urología, dermatología, ortopedia, neurología, ginecología, oftalmología, pediatría, hematología y pacientes críticos, así como métodos de diagnóstico. . Se hace especial referencia a consideraciones legales y éticas como precisión, consentimiento informado, cuestiones de privacidad, seguridad de los datos, marco regulatorio, responsabilidad del producto, explicabilidad y transparencia. Finalmente, esta revisión cierra valorando críticamente el uso de la IA en la práctica clínica y sus perspectivas futuras. Sin embargo, también es importante abordar su desarrollo e implementación con cautela para garantizar que se cumplan las consideraciones éticas.
Palabras clave: inteligencia artificial ; Práctica clinica ; aprendizaje automático ; Redes neuronales ; decisión clínica ; Medicina personalizada
1. Introducción
La inteligencia artificial (IA) se refiere a la emulación de la inteligencia humana en máquinas diseñadas para exhibir habilidades cognitivas y adquirir conocimientos similares a los de los seres humanos [ 1 , 2 ]. Los antiguos griegos atribuían un carácter distintivo a los seres humanos en virtud de su posesión de facultades de razonamiento. La noción de alma fue introducida por varios eruditos religiosos, quienes la postularon como una esencia intrínseca y duradera otorgada a la humanidad por un creador divino [ 3 ]. Según Platón, es concebible que un individuo posea inteligencia y al mismo tiempo carezca de conocimientos sustanciales sobre el mundo exterior o, más significativamente, sobre sí mismo. Aristóteles, alumno de Platón, fue pionero en la formulación de un conjunto distinto de principios que gobiernan el aspecto lógico de la cognición humana. En 1936, Alan Turing escribió un artículo académico en el que aclaraba el concepto de “ Entscheidungsproblem ” y exponía la noción de “calculabilidad efectiva” como medio para abordar este dilema. Los autores sentaron las bases para los modelos computacionales conocidos como algoritmos [ 4 ]. El desarrollo inicial de una red neuronal artificial (RNA) compuesta de circuitos eléctricos se produjo en 1943, con el objetivo de simular las interacciones entre las neuronas del cerebro [ 5 ]. Los inicios de la IA tuvieron lugar en 1956 en el Dartmouth College. Después de un lapso de tres años, la investigación informática inicial utilizando una ANN se llevó a cabo con éxito, utilizando modelos denominados «Adaline» y «Madaline» [ 6 ]. El diagnóstico asistido por ordenador se implementó inicialmente en el examen de los nódulos pulmonares identificados en radiografías de tórax en 1963 [ 7 ]. Los investigadores hicieron una observación importante sobre la aplicabilidad de la IA en el campo de las biociencias aproximadamente quince años después de su inicio. Esta observación fue particularmente evidente en los experimentos de Dendral [ 8 ]. Sin embargo, la utilización de la IA en el campo de la medicina se vio limitada por limitaciones tecnológicas hasta 1998, cuando la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó el primer sistema de detección asistida por computadora (CAD) de mamografía [ 9 ]. En la Figura 1 se muestra una representación esquemática de algunos hitos importantes en la evolución de la IA .
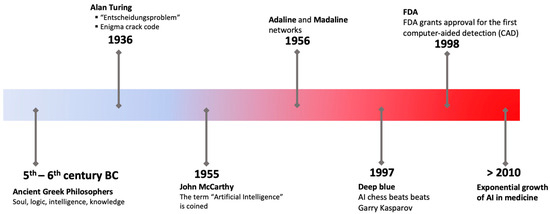
Figura 1. La progresión de conceptos en inteligencia artificial e hitos importantes. Hoy en día, como afirma el grupo de expertos en IA dentro de la estrategia digital de la Comisión Europea, los sistemas de IA se refieren a sistemas de software y potencialmente de hardware. Estos sistemas están diseñados para operar en condiciones físicas o digitales, con la capacidad de percibir su entorno mediante la adquisición de datos. En los últimos años, ha habido un progreso significativo en la IA, lo que ha llevado a su adopción generalizada en diversas industrias, como la atención médica, las finanzas, el transporte, el descubrimiento de fármacos y, más recientemente, en la farmacocinética [ 10 , 11 , 12 , 13 , 14 , 15 , 16]. , 17 , 18 , 19 , 20 , 21 , 22 ]. En los últimos años, se han logrado avances notables en el campo de la IA, caracterizado por la aparición de algoritmos y programas informáticos que exhiben capacidades cognitivas similares a las humanas. Un área donde la IA se ha mostrado muy prometedora es en la práctica clínica [ 23 ]. La incorporación de la IA en entornos clínicos introduce una serie de ventajas y desafíos, acompañada de implicaciones notables para consideraciones éticas y legales [ 1 ]. La IA tiene el potencial de mejorar la precisión del diagnóstico, agilizar las tareas administrativas y personalizar los planes de tratamiento. Mediante el análisis de datos médicos extensos, los sistemas de inteligencia artificial pueden discernir patrones y correlaciones que pueden eludir la observación humana, lo que lleva a intervenciones más precisas y oportunas [ 1 , 2 ]. Además, la IA tiene la capacidad de contribuir a soluciones sanitarias rentables y, en última instancia, mejorar los resultados generales de los pacientes. La integración de la tecnología de inteligencia artificial facilita los procesos de toma de decisiones clínicas informadas, lo que promete avances como diagnósticos más rápidos y precisos, planes de tratamiento personalizados y costos de atención médica reducidos. Si bien los beneficios potenciales de la IA en la práctica clínica son sustanciales, surgen complejidades éticas y legales. La utilización de la IA en la toma de decisiones clínicas genera preocupaciones sobre la transparencia, la responsabilidad y el posible sesgo dentro de los algoritmos. Salvaguardar la privacidad del paciente y garantizar la seguridad de los datos se vuelve crucial, lo que requiere directrices éticas y marcos legales sólidos. Lograr un delicado equilibrio entre fomentar la innovación y proteger los derechos de los pacientes requiere una consideración cuidadosa de las implicaciones éticas de la IA en la práctica clínica, junto con el desarrollo de marcos legales adaptables capaces de seguir el ritmo de los avances tecnológicos en el sector de la salud. Abordar los desafíos éticos y legales de la integración de la IA en la práctica clínica exige un enfoque integral que abarque marcos y regulaciones legales, IA transparente y explicable, pautas y estándares éticos, auditorías y evaluaciones periódicas, incentivos para prácticas éticas y colaboración internacional. Esta revisión de la literatura tiene como objetivo proporcionar una sinopsis fundamental de la investigación actual sobre la IA en el ámbito de la práctica clínica. Además del papel generalizado de la IA en los métodos de diagnóstico, también se analizan las aplicaciones de la IA en varias especialidades médicas como cardiología, anestesiología, cirugía, neumología, neurología, urología, ginecología, hematología y pediatría. Cabe destacar que el propósito de esta revisión no es únicamente proporcionar una sinopsis de un campo específico (por ejemplo, especialidad), sino más bien intentar ofrecer una visión general de las aplicaciones actuales de la IA en medicina.
2. Materiales y métodos
El alcance de esta investigación se limitó a artículos escritos en inglés y sujetos a revisión por pares que cumplieran al menos uno de los siguientes requisitos previos: (a) haber sido publicados dentro del plazo de los últimos diez años y (b) ser artículos fundamentales en el campo. de IA que construyó lo que hoy conocemos como inteligencia artificial. Se realizó una búsqueda bibliográfica utilizando las bases de datos PubMed y Scopus desde el 14 de julio de 2023 hasta el 31 de agosto de 2023. Además, se consultaron libros de texto sobre IA. Se utilizaron dos conjuntos de palabras clave para reconocer términos dentro del título, resumen y palabras clave de los artículos.
- El conjunto inicial de palabras clave incluía términos asociados con la inteligencia artificial, como «inteligencia artificial», «aprendizaje automático» y «aprendizaje profundo». Sin embargo, es muy probable que las investigaciones que utilizan estas metodologías incorporen términos como “inteligencia artificial” o “aprendizaje automático” en sus resúmenes o palabras clave;
- El siguiente conjunto de palabras clave abarcó conceptos asociados con la aplicación en la práctica clínica y el estatus legal. En este caso, se realizaron búsquedas compuestas utilizando los términos “inteligencia artificial” Y la especialidad médica: “cardiología”, “cirugía”, “anestesiología”, “gastroenterología y hepatología”, “neumonología”, “nefrología”, “urología”, “dermatología”, “ortopedia”, “neurología”, “ginecología, “oftalmología”, “pediatría”, “hematología”, “unidad de cuidados intensivos”, “métodos de diagnóstico”, “estatus jurídico”, “responsabilidad”, “marco regulatorio ”.
Tras la eliminación de entradas duplicadas, se realizó una evaluación exhaustiva de los títulos y resúmenes de los artículos identificados para determinar su idoneidad para su inclusión: Se aplicaron sistemáticamente los criterios de selección para la evaluación de los estudios. Luego de eliminar los artículos duplicados, el autor evaluó cada estudio con base en los siguientes criterios: (i) revista, (ii) autoría, (iii) fecha de publicación, (iv) diseño del estudio, (v) métodos de análisis, (vi) resultados, y (vii) conclusiones. Los criterios de elegibilidad abarcaron artículos escritos en inglés pertinentes a los objetivos de la revisión. Se realizó una selección inicial de resúmenes, excluyendo los estudios que no cumplían con los criterios de elegibilidad. Para mejorar la calidad de los datos, todos los estudios que cumplieron con los criterios de inclusión se sometieron a una evaluación integral, centrándose en aspectos como la justificación, el diseño del método, los resultados, la discusión y las conclusiones. Posteriormente se excluyeron los estudios que presentaban cualquier sesgo en la metodología, los resultados o la interpretación de los datos que pudiera afectar el resultado general.Los criterios de exclusión abarcaron lo siguiente: (a) estudios que se centraron exclusivamente en el avance y la verificación de algoritmos clínicos de IA sin ninguna implementación tangible y (b) aplicaciones de IA que proporcionaron predominantemente funcionalidades de automatización, como la administración y el monitoreo automatizados de insulina, como opuesto a ofrecer apoyo para la toma de decisiones.
3. Resultados
3.1. General
La inteligencia artificial ha revolucionado el campo de la medicina y la atención sanitaria al proporcionar soluciones innovadoras a problemas complejos [ 1 , 5 ]. Existen varios tipos de IA, incluido el aprendizaje profundo (DL), el aprendizaje automático (ML) y el lenguaje natural ( Figura 2 ). DL es un subconjunto de inteligencia artificial que se centra en entrenar redes neuronales para aprender y tomar decisiones de manera similar al cerebro humano ( Figura 3 ). Los algoritmos DL están diseñados para aprender y mejorar a partir de la experiencia automáticamente, sin la necesidad de programación explícita [ 24 , 25 , 26 ]. Esta capacidad de analizar grandes cantidades de datos y extraer patrones significativos ha convertido a DL en una herramienta poderosa en campos como el reconocimiento de imágenes y la conducción autónoma.
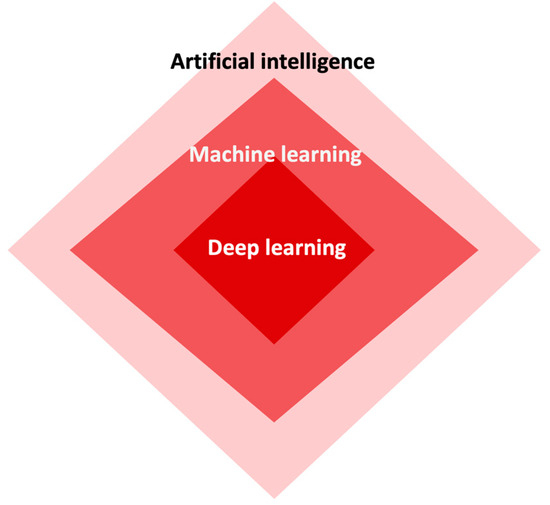
Figura 2. La interconexión entre inteligencia artificial, aprendizaje automático y aprendizaje profundo.

Figura 3. Representación esquemática de una red neuronal artificial. El aprendizaje automático se centra principalmente en el avance de algoritmos y modelos que permiten a las computadoras adquirir conocimientos y generar predicciones o decisiones de forma autónoma sin la necesidad de programación explícita [ 2 ]. El ML se puede clasificar en términos generales en varias categorías, como aprendizaje supervisado, no supervisado y por refuerzo (consulte la Tabla 1 ). En el aprendizaje supervisado, un algoritmo aprende de datos etiquetados para hacer predicciones o decisiones [ 2 ]. Este enfoque entrena el algoritmo en un conjunto de datos que comprende variables de entrada y sus correspondientes variables de salida. El objetivo es permitir que el algoritmo comprenda la relación entre las variables de entrada y salida, facilitando así predicciones precisas para instancias de datos novedosos y no observados. Se utilizan habitualmente varios algoritmos de aprendizaje supervisado, incluida la regresión lineal, la regresión logística, las máquinas de vectores de soporte y los árboles de decisión.
Tabla 1. Una clasificación común de algoritmos de aprendizaje automático.

El aprendizaje no supervisado representa un subcampo distinto dentro del aprendizaje automático, donde el algoritmo funciona sin la presencia de datos etiquetados [ 2 , 24 , 27 , 28 ]. En cambio, su propósito es identificar de forma autónoma patrones, estructuras o relaciones dentro de los datos. Este tipo de aprendizaje resulta muy ventajoso cuando no existe una variable objetivo definitiva o cuando el objetivo es extraer información valiosa de los datos sin predicciones predeterminadas. Los algoritmos de aprendizaje no supervisados incluyen varios métodos, como algoritmos de agrupamiento como k-means y agrupamiento jerárquico, así como técnicas de reducción de dimensionalidad como PCA y análisis factorial.
El objetivo principal del aprendizaje por refuerzo es capacitar a agentes autónomos para tomar efectivamente una serie de decisiones dentro de un entorno determinado, con el objetivo de optimizar la recompensa acumulada total obtenida [ 29 ].
A diferencia del aprendizaje supervisado, donde el agente recibe datos etiquetados, o del aprendizaje no supervisado, donde el agente aprende patrones y estructuras a partir de datos no etiquetados, el aprendizaje por refuerzo opera según el principio de prueba y error. Ejemplos de enfoques de aprendizaje por refuerzo incluyen los métodos basados en valores (p. ej., Q-learning y SARSA), los métodos basados en políticas (p. ej., gradiente de políticas y refuerzo) y métodos basados en modelos (p. ej., búsqueda de árbol de Monte Carlo).El procesamiento del lenguaje natural (PNL) es un campo de estudio que se centra en examinar y comprender la interacción entre los sistemas informáticos y el lenguaje humano [ 2 ].
El campo de estudio pertenece al avance de algoritmos y metodologías que facilitan que las máquinas comprendan, interpreten y produzcan el lenguaje humano de una manera que posea significado y utilidad. La PNL se ha vuelto cada vez más importante en nuestra era digital, ya que permite a las computadoras procesar y analizar grandes cantidades de datos de texto, como correos electrónicos, publicaciones en redes sociales y artículos de noticias, para extraer conocimientos e información valiosos.
Una de las principales ventajas de la IA en la práctica clínica es su capacidad para analizar de forma rápida y precisa grandes volúmenes de datos. Esta capacidad ha dado lugar a una variedad de aplicaciones que no sólo han mejorado los resultados de los pacientes sino que también han reducido la carga de trabajo de los profesionales de la salud [ 30 ]. En esta sección, exploraremos algunas de las aplicaciones más prometedoras de la IA en la práctica clínica. La evolución de la IA ha experimentado cambios significativos en las últimas décadas.
La llegada del aprendizaje automático (ML) y el aprendizaje profundo (DL) ha ampliado las aplicaciones en el campo de la inteligencia artificial en la medicina, allanando el camino para la medicina personalizada en lugar de depender únicamente de enfoques algorítmicos.
El uso de modelos predictivos es prometedor para aplicaciones en el diagnóstico de enfermedades, la predicción de la respuesta terapéutica y, potencialmente, el avance del campo de la medicina preventiva en los próximos años. La IA tiene el potencial de mejorar la precisión del diagnóstico, optimizar el flujo de trabajo de los proveedores de atención médica y las operaciones clínicas, facilitar un seguimiento más eficaz de las enfermedades y terapias, mejorar la precisión de los procedimientos médicos y, en última instancia, mejorar los resultados de los pacientes.
3.2. Cardiología
La aplicación de sofisticados algoritmos computacionales y técnicas de aprendizaje automático en el campo de la cardiología se denomina comúnmente IA. Este enfoque tiene como objetivo analizar e interpretar datos cardíacos de una manera más avanzada y eficiente. Implica el desarrollo de sistemas inteligentes que puedan aprender de los datos, hacer predicciones y ofrecer información valiosa para ayudar en el diagnóstico, tratamiento y manejo de enfermedades cardiovasculares. En la actualidad, existen dos posiciones distintas para la IA en el ámbito de las imágenes cardiovasculares [31 ]. La automatización se refiere al proceso de reemplazar la participación humana en diversas tareas, incluidas, entre otras, la segmentación de imágenes y la evaluación de parámetros estructurales y funcionales. Otro aspecto importante es la identificación de conocimientos que tengan importancia clínica. La mayoría de las aplicaciones documentadas se centraron principalmente en la implementación de la automatización de tareas. Además, ha habido informes sobre el desarrollo de algoritmos capaces de adquirir mediciones cardíacas. La IA ha tenido un impacto significativo en varias facetas de las imágenes cardiovasculares, cubriendo todo el espectro desde la adquisición de datos iniciales hasta la fase de informe final [ 32 , 33 ]. Ejemplos de este impacto incluyen el uso de la IA en el avance de las técnicas de tomografía computarizada y resonancia magnética para medir el diámetro de la luz, reconocer la puntuación de calcio coronario e identificar la enfermedad coronaria obstructiva. Además, la IA ha sido fundamental para automatizar procesos como la adquisición, la segmentación y la generación de informes [ 34 ,35 ]. A diferencia de las metodologías mencionadas anteriormente, surge una preocupación notable con respecto a la sustancial variabilidad del observador observada en la interpretación de los ecocardiogramas. La IA tiene el potencial de abordar este problema mitigando la variabilidad entre observadores y mejorando la precisión diagnóstica dentro del campo de la ecocardiografía. En los últimos años, se han realizado numerosos estudios para investigar la detección de miocardiopatía, con especial atención a la utilización de la IA junto con la electrocardiografía (ECG) para mejorar las capacidades de diagnóstico [ 36 , 37 ]. La viabilidad del uso conjunto de IA/ECG para la detección de amiloidosis, miocardiopatía y miocardiopatía dilatada permanece intacta, incluso en casos de disfunción ventricular izquierda leve [ 38 , 39 ]. La aplicación de IA/ECG en la práctica clínica habitual ha aumentado la identificación de disfunción sistólica del ventrículo izquierdo. En imágenes, la IA se utiliza para evaluar automáticamente el grosor y las propiedades del miocardio para distinguir entre diferentes tipos de miocardiopatías [ 39 , 40 ]. Sin embargo, actualmente faltan investigaciones que investiguen el potencial de pronóstico de esta tecnología de IA. La IA también se está utilizando en la genómica de la miocardiopatía, particularmente para predecir la patogenicidad de variantes genéticas y determinar su relevancia clínica [ 41 , 42 , 43 ].
3.3. Cirugía
La aplicación de modelos de IA y ML tiene un potencial significativo en el campo de la cirugía. Estos modelos demuestran aplicaciones prometedoras tanto en la fase preoperatoria, diagnosticando con precisión las afecciones pancreáticas, como en la fase posoperatoria, evaluando el pronóstico y prediciendo complicaciones [ 44 , 45 , 46 ].
La IA también ha demostrado ser beneficiosa para ayudar en las cirugías bariátricas. La creciente integración de las tecnologías de IA en diversas subespecialidades de la atención sanitaria ha dado lugar a avances prometedores en su aplicación en la cirugía bariátrica [ 47 , 48 ]. El manejo de pacientes candidatos a cirugía bariátrica es un tema complejo. El proceso de evaluación requiere la participación de un equipo multidisciplinario compuesto por profesionales de diversos campos, incluidos internistas, psiquiatras, cirujanos generales y anestesiólogos. Los médicos de diversas especialidades médicas participan en la evaluación integral de los pacientes antes, durante y después de los procedimientos quirúrgicos, una tarea que presenta dificultades considerables debido a la naturaleza compleja de las personas que padecen obesidad [ 49 ].
Existen numerosas aplicaciones potenciales de la IA durante el período intraoperatorio. Tiene el potencial de utilizarse en el manejo de la farmacoterapia, la optimización hemodinámica, la monitorización del bloqueo neuromuscular y la evaluación de la profundidad de la anestesia [ 50 ]. Uno de los informes más notables se refiere a la predicción de la cinética de distribución temprana del propofol. De hecho, el volumen de distribución de fármacos en personas con obesidad está sujeto a modificaciones. En concreto, se produce un aumento del volumen sanguíneo y del gasto cardíaco, junto con alteraciones en las proteínas de transporte plasmáticas. Un estudio utilizó IA para manejar la cinética de la fase de inducción de manera efectiva [ 51 ]. Esto se logró mediante la utilización de un conjunto de datos farmacocinéticos completos con alta resolución. Se realizó un análisis comparativo para evaluar el rendimiento de un modelo tradicional de cuatro compartimentos, un modelo recirculatorio y una red neuronal unitaria recurrente cerrada. El estudio concluyó que tanto un modelo recirculatorio como una unidad recurrente cerrada de ANN demostraron un rendimiento similar, superando a un modelo compartimental en la representación precisa de datos farmacocinéticos de alta resolución del propofol [ 51 ].En el mismo contexto, los cirujanos plásticos se encuentran frecuentemente con escenarios clínicos que carecen de soluciones definitivas. Para lograr un enfoque de tratamiento ideal es necesario utilizar un modelo de decisión integral que incorpore de manera efectiva varios factores influyentes, incluidos datos clínicos y demográficos.
Antes de la llegada de la IA, la técnica de análisis del árbol de decisión se utilizaba habitualmente para construir dichos modelos. La localización de puntos de referencia anatómicos importantes en imágenes médicas juega un papel crucial en la planificación preoperatoria y la evaluación de los resultados posoperatorios [ 52 ]. Sin embargo, el proceso de identificación actual se lleva a cabo manualmente o ejecutando los auxiliares insertados, lo que resulta en un procedimiento lento e impreciso. Para mejorar la precisión de la localización de puntos de referencia en la superficie distal del fémur, los científicos idearon un algoritmo que inicialmente transformaba imágenes tridimensionales en tres conjuntos distintos de imágenes bidimensionales [ 52 ]. Posteriormente, el algoritmo adquirió la capacidad de reconocer puntos de referencia dentro de estas imágenes y posteriormente integró estos resultados para determinar con precisión las coordenadas espaciales de los puntos de referencia identificados en tres dimensiones.
3.4. Anestesiología
La aplicación de la IA ha producido resultados notables en la anestesia y el manejo de quirófanos [ 53 , 54 ]. A lo largo de cada fase del proceso perioperatorio, específicamente las fases preoperatoria [ 55 , 56 , 57 ], intraoperatoria [ 16 , 17 , 18 , 19 , 20 ] y postoperatoria [ 42 , 44 ], se pueden ejecutar distintas tareas utilizando diversas técnicas. La eficacia de una red neuronal diseñada para identificar la intubación esofágica se vuelve innecesaria en presencia de capnografía continua [ 58 , 59 ]. En este caso, un examen clínico fiable ha revelado una complicación previamente oculta y muy perjudicial. El uso de video laringoscopia requiere el ajuste de un modelo ML diseñado para predecir una intubación difícil según la apariencia del paciente. La expansión de la tecnología de gestión de las vías respiratorias ha dado lugar a un mayor espectro de resultados aceptables en términos de visualización laríngea. Desde la década de 1950, el concepto de un algoritmo que regule de forma autónoma la profundidad de la anestesia mediante registros EEG ha sido objeto de investigación continua. Los anestesiólogos han explorado esta posibilidad durante un período considerable, pero continúa siendo un área de investigación activa.
3.5. Gastroenterología y Hepatología
El campo de la gastroenterología y la hepatología está experimentando un crecimiento significativo en la implementación potencial de técnicas de IA y ML. En los últimos años, ha habido un creciente conjunto de investigaciones centradas en examinar las aplicaciones de la IA en diversos contextos médicos, en particular la utilización del diagnóstico asistido por computadora (CAD). Estas aplicaciones abarcan el uso de CAD en el diagnóstico de lesiones gastrointestinales premalignas y malignas, la predicción de la respuesta al tratamiento en pacientes con enfermedad inflamatoria intestinal, la realización de análisis histopatológicos de muestras de biopsia, la evaluación de la gravedad de la fibrosis hepática en personas con enfermedad hepática crónica y el desarrollo de modelos para trasplante de hígado. asignación y exploración de otras áreas relacionadas [ 60 ].El ámbito de la prevención y detección temprana del cáncer de esófago muestra un potencial significativo de avances mediante la utilización de la IA. Se han logrado avances sustanciales en la investigación en este campo, con una parte notable de la investigación sobre el cáncer de esófago en los Estados Unidos dedicada a la investigación de tecnologías, incluidas aquellas que involucran IA, destinadas a mejorar la detección temprana y el tratamiento del esófago de Barrett y el adenocarcinoma de esófago [ 61 , 62] . ]. La IA posee la capacidad de asumir un papel importante en el proceso de toma de decisiones para el tratamiento de la enfermedad inflamatoria intestinal al predecir con precisión la respuesta al tratamiento en una etapa anterior y brindar orientación para la selección de terapia personalizada. Dentro del campo de la enfermedad inflamatoria intestinal, los investigadores han logrado avances en el desarrollo de herramientas de visión por computadora AI/ML. Estas herramientas han sido diseñadas específicamente para evaluar la gravedad de las enfermedades mediante examen endoscópico. Los principales objetivos de su estudio implican la diferenciación de colitis de neoplasia y la distinción entre adenomas esporádicos y lesiones no neoplásicas. Se han entrenado algoritmos de IA para pronosticar la respuesta al tratamiento y evaluar la probabilidad de recurrencia de la enfermedad [ 63 , 64 ]. Existen numerosas aplicaciones potenciales para la IA y el ML en el ámbito de la hepatología. Los objetivos anteriores abarcan la evaluación de la progresión de la fibrosis hepática, la identificación de la enfermedad del hígado graso no alcohólico, el reconocimiento de personas en riesgo de desarrollo de carcinoma hepatocelular y la mejora de los protocolos para el trasplante de órganos [ 65 , 66 ].La prevención y el control del cáncer colorrectal representan importantes esfuerzos de salud pública realizados por los gastroenterólogos. Los avances realizados en el campo del ML han dado como resultado la utilización de técnicas de visión por computadora para ayudar en la detección de pólipos durante los procedimientos de colonoscopia. La evidencia empírica ha demostrado la eficacia de los sistemas CAD para mejorar la tasa de detección de adenomas [ 67 , 68 , 69 , 70 ].
3.6. Neumonología
La IA, específicamente la utilización de algoritmos DL y ML para el reconocimiento de patrones, es muy prometedora para diversas aplicaciones dentro del campo de la medicina pulmonar. Estas aplicaciones abarcan análisis de imágenes, procesos de toma de decisiones y predicción de pronósticos [ 5 , 6 , 7 ]. El cáncer de pulmón es una neoplasia maligna prevalente caracterizada por importantes tasas de morbilidad y mortalidad clínica [ 71 ]. Los nódulos pulmonares son las manifestaciones imagenológicas predominantes observadas durante la fase inicial del cáncer de pulmón, lo que plantea desafíos para la interpretación manual de las películas. La tecnología de reconocimiento de IA puede realizar análisis de grupos multiparamétricos y agilizar el procesamiento de imágenes, ayudando así a los profesionales médicos en la detección temprana del cáncer de pulmón [ 72 ]. En los últimos años, los informes han indicado que los sistemas de IA han demostrado la capacidad de identificar nódulos pulmonares malignos mediante el análisis de imágenes de tomografía computarizada (TC) de tórax [ 73 ].
El modelo se desarrolló utilizando tecnología DL y la IA se utiliza para el análisis de películas de TC con el fin de ayudar a los profesionales médicos a mejorar la precisión de la detección del cáncer de pulmón. Otro estudio construyó un modelo predictivo aplicando análisis de regresión logística, integrando marcadores tumorales específicos en el modelo [ 74 ]. Los resultados del estudio demostraron que el modelo predictivo desarrollado mostró un rendimiento significativamente mejor en comparación con la estrategia básica de detección combinada que involucra marcadores tumorales.
Las investigaciones han demostrado que la IA puede mejorar potencialmente la predicción del riesgo quirúrgico, facilitando así la selección del abordaje quirúrgico más óptimo [ 75 , 76 ]. Un ejemplo de sistema de computación cognitiva, IBM Watson for Oncology, utiliza técnicas de inteligencia artificial para el análisis de datos y la conversión de imágenes. Su objetivo principal es ayudar a los profesionales médicos a identificar de manera eficiente información crucial en los registros médicos de los pacientes, presentar evidencia pertinente y facilitar la exploración de posibles opciones de tratamiento [ 77 ]. La aplicación de redes neuronales profundas en la identificación de enfermedades respiratorias, específicamente en radiografías de tórax y tomografías computarizadas, ha dado como resultado una mejora notable en la precisión diagnóstica en comparación con características subjetivas como la especulación tumoral, así como características objetivas como la forma y textura adquiridas a través de software de análisis de imágenes [ 78 ].
3.7. Nefrología
El concepto de inmunoglobulina progresiva se refiere al desarrollo y maduración gradual de las inmunoglobulinas y la nefropatía por IgA (NIgA) es una etiología reconocida de insuficiencia renal. Sin embargo, la capacidad del nefrólogo para anticipar la aparición de insuficiencia renal entre los pacientes en el momento del diagnóstico es un desafío. Sin embargo, la capacidad de discernir a estos individuos resultaría ventajosa desde el punto de vista del pronóstico y del tratamiento. Se ha postulado la existencia de una función que establece una relación entre parámetros clínicos y biológicos, como edad, sexo, presión arterial, proteinuria, nivel de creatinina sérica y tratamientos antihipertensivos, en el momento del diagnóstico de NIgA y la probabilidad de desarrollando NIgA progresiva [ 79 ]. Los investigadores idearon y ejecutaron el desarrollo de una RNA con el propósito de aproximar la función antes mencionada. Los hallazgos indicaron que la ANN demostró una precisión superior en la predicción de la aparición de NIgA progresiva en comparación con nefrólogos experimentados [ 79 ]. En concreto, la RNA logró predicciones correctas en el 87% de los casos, mientras que los nefrólogos lograron una tasa de precisión inferior, del 69,4%. Además, la ANN mostró una sensibilidad mayor del 86,4% en comparación con la sensibilidad de los nefrólogos del 72%, lo que indica su capacidad para identificar correctamente los casos verdaderos positivos. De manera similar, la ANN mostró una especificidad mayor del 87,5% en comparación con la especificidad de los nefrólogos del 66%, lo que indica su capacidad para identificar con precisión casos verdaderos negativos. Estos enfoques pueden utilizarse potencialmente en una amplia gama de enfermedades progresivas, ayudando así a los médicos en el proceso de estadificación y tratamiento del paciente. Los modelos de IA se han aplicado para diversos fines, incluida la predicción de la tasa de disminución de la tasa de filtración glomerular en personas con poliquistosis renal autosómica dominante, la mejora del tratamiento de la anemia en pacientes en hemodiálisis, la estimación de una duración adecuada de la diálisis para lograr el nivel deseado de eliminación de urea, determinar el peso seco óptimo en pacientes sometidos a hemodiálisis e identificar patógenos específicos responsables de infecciones bacterianas en pacientes con enfermedad de Parkinson [ 80 , 81 , 82 , 83 ].
3.8. Urología
La IA se utiliza predominantemente en el campo de la urología, particularmente en el ámbito de las neoplasias malignas genitourinarias. En un estudio, se utilizó IA para predecir los resultados de las biopsias de próstata, con un enfoque específico en el cáncer de próstata. Se aplicaron algoritmos de ML para analizar la probabilidad libre de recurrencia y la evaluación diagnóstica del cáncer de vejiga. Ha habido informes anecdóticos sobre la estadificación y predicción de la recurrencia de la enfermedad en casos de cáncer de riñón y testículo. Recientemente, la IA ha encontrado aplicación en enfermedades no oncológicas, específicamente en áreas como los cálculos y la urología funcional.En las últimas décadas, numerosas investigaciones académicas han examinado la utilización de la IA en el tratamiento del cáncer de próstata. Estos estudios se alinean con el paradigma contemporáneo de la medicina y la cirugía de precisión [ 84 ]. El diagnóstico del cáncer de próstata abarca una amplia gama de aplicaciones, que han experimentado numerosos avances en los últimos años [ 85 ]. En 1994 se realizó un estudio fundamental para determinar la utilidad potencial de las RNA en la predicción de los resultados de la biopsia en hombres que presentaban niveles anormales del antígeno prostático específico. Además, el estudio tuvo como objetivo evaluar la eficacia de la ANN para predecir los resultados del tratamiento después de una prostatectomía radical [ 85 , 86 ]. Un estudio demostró la precisión predictiva de dos sistemas de IA distintos [ 87 ]. Estos sistemas se diseñaron específicamente utilizando datos de bases de datos de referencias europeas multicéntricas con sede en Viena. Estos sistemas de IA tienen como objetivo facilitar la detección temprana del cáncer de próstata en hombres. Otro estudio encontró que un modelo de supervivencia DL exhibía la capacidad de predecir el período de recuperación de la continencia urinaria después de la prostatectomía radical asistida por robot [ 88 ]. Esta predicción se logró incorporando marcadores de patología anatómica (MAP) y factores relacionados con el paciente. Además, este modelo en particular ha identificado con éxito las APM de los mejores cirujanos que pueden clasificarlos de manera efectiva, superando la capacidad predictiva de la experiencia del cirujano por sí sola. Los APM pudieron diferenciar a los cirujanos según la calidad de la recuperación de la continencia urinaria observada en sus pacientes, distinguiendo entre aquellos con resultados superiores e inferiores. En un estudio fundamental hace veinte años, los autores realizaron un análisis comparativo de los modelos de regresión de Cox e IA para predecir la recurrencia de la enfermedad después de la cirugía [ 89 ]. Los resultados del estudio demostraron que los modelos de regresión de Cox mostraron un rendimiento superior en este sentido. Junto con la creciente variedad de indicaciones quirúrgicas para el cáncer de riñón metastásico, se realizó un estudio para evaluar la capacidad predictiva de la IA para determinar el pronóstico de pacientes con carcinoma de células renales metastásico que inician una terapia sistémica [ 90 ]. Los investigadores proporcionaron a su sistema de inteligencia artificial un conjunto de datos que constaba de información de 175 pacientes que se habían sometido a una nefrectomía del tumor primario antes de recibir terapia sistémica. El objetivo de este estudio fue pronosticar la tasa de supervivencia global tres años después de iniciar el tratamiento inicial, utilizando parámetros accesibles al comienzo del tratamiento de primera línea. La IA ha demostrado el potencial de lograr una precisión de predicción del 95 % en la predicción de las tasas de supervivencia general. Este desempeño supera los modelos de regresión, lo que indica la posible aplicación futura de la IA como herramienta de estratificación de riesgos. Una infección del tracto urinario es una infección bacteriana común que afecta el sistema urinario, incluidas la vejiga y la uretra. Un estudio notable se centró en las infecciones del tracto urinario donde se desarrolló un sistema de inteligencia artificial para ayudar en el diagnóstico de dichas infecciones [ 91 ]. En el estudio participaron personas diagnosticadas con cistitis o uretritis inespecífica. Los sujetos se sometieron a varios procedimientos, incluida una evaluación de la historia clínica, un examen físico, análisis de muestras de orina y el uso de ecografía. Los hallazgos demostraron la eficacia de la IA en el diagnóstico de infecciones del tracto urinario basándose únicamente en los valores de eritrocitos junto con síntomas como dolor suprapúbico, polaquiuria y resultados de análisis de orina. El modelo de IA mostró una tasa de precisión notablemente alta del 98,3%, lo que sugiere que podría servir como una alternativa rentable a las costosas pruebas de laboratorio y de ultrasonido. La urología funcional se refiere a la rama de la urología que se centra en el estudio y manejo del tracto urinario. La exploración de posibles aplicaciones de la IA también se ha extendido al ámbito de la urología funcional. Un estudio comparó un modelo de IA y una regresión lineal múltiple en términos de su eficacia para reemplazar la evaluación urodinámica preoperatoria en mujeres diagnosticadas con prolapso de órganos pélvicos [ 92 ]. Un total de 804 mujeres diagnosticadas con prolapso de órganos pélvicos fueron sometidas a un examen, lo que reveló que se determinó que tanto la regresión logística multivariada como la IA eran menos efectivas que los estudios urodinámicos para evaluar la disfunción urinaria. Un trasplante de riñón es un procedimiento quirúrgico en el que se trasplanta un riñón sano de un donante a un receptor. En los últimos años, ha habido un interés creciente en la utilización de herramientas predictivas de IA en el trasplante de riñón. De manera similar, se ha explorado la posible aplicación de la IA para identificar factores de riesgo y covariables que contribuyen al fracaso del trasplante renal [ 93 ]. El enfoque de IA se comparó con el modelo de regresión logística tradicional. El método de IA demostró una precisión superior en comparación con la regresión logística, como lo demuestra el análisis de datos de 378 pacientes.
3.9. Dermatología
La identificación de enfermedades de la piel se basa principalmente en los atributos aparentes que exhiben las lesiones. Sin embargo, la dermatología abarca una amplia colección de más de 2000 tipos distintos de enfermedades dermatológicas. Ciertas lesiones cutáneas asociadas con diversas enfermedades pueden presentar similitudes, lo que plantea desafíos para un diagnóstico y tratamiento precisos [ 94 , 95 ]. En particular, existe una escasez significativa de dermatólogos, particularmente en los países en desarrollo y regiones remotas, donde se necesitan con urgencia mayores recursos médicos, consultas profesionales y apoyo clínico [ 96 , 97 ].La convergencia de la rápida iteración de big data, los avances en la tecnología de reconocimiento de imágenes y la proliferación global de teléfonos inteligentes presentan un potencial transformador para el diagnóstico y tratamiento de enfermedades de la piel [ 98 , 99 ]. La IA, en particular, tiene la capacidad de ofrecer diagnósticos rápidos, facilitando una gama más amplia de opciones de tratamiento y mejorando la accesibilidad, especialmente para regiones marginadas e individuos con recursos limitados [ 100 ]. La integración de la tecnología y los algoritmos de IA tiene el potencial de establecerse rápidamente como un enfoque estándar en el campo del diagnóstico y la evaluación. El examen de la estructura y forma de una anomalía cutánea es un aspecto fundamental del diagnóstico dermatológico. Los avances en IA han llevado a mejoras significativas en el reconocimiento facial y el análisis estético, haciéndolos más confiables [ 101 ].Los inicios de la IA en el campo de la dermatopatología se remontan a 1987, cuando se utilizó en una computadora personal un sistema basado en texto conocido como TEGUMENT. El sistema fue desarrollado específicamente con el propósito de clasificar 986 diagnósticos histopatológicos basados en imágenes de microscopio óptico. Demostró una precisión diagnóstica del 91,8% en comparación con las evaluaciones realizadas por un dermatopatólogo calificado [ 102 ]. Durante ese período de tiempo particular, la ausencia de equipos y tecnologías necesarios para obtener imágenes de diapositivas completas llevó a la creencia de que la noción de análisis de imágenes independiente del ser humano no era viable. En los últimos años, la clasificación precisa de los diagnósticos de rutina mediante sistemas basados en máquinas se ha convertido en una realidad tangible [ 103 ].En un estudio de investigación, se desarrollaron 11 algoritmos DL para identificar y clasificar imágenes en portaobjetos completos de nevo dérmico, queratosis seborreica y carcinoma nodular de células basales [ 104 ]. Las representaciones visuales sufrieron un proceso de pixelación, dando como resultado la desintegración de las imágenes, que posteriormente fueron sometidas a análisis de datos. Se desarrolló un algoritmo DL para patología que incorpora imágenes de portaobjetos completos. El algoritmo clasifica eficazmente estas imágenes en cuatro grupos de diagnóstico distintos: basaloide, escamoso, melanocítico y otros. El sistema implementado utiliza una serie de tres redes neuronales convolucionales consecutivas para determinar el diagnóstico con la mayor probabilidad.La distinción entre lesiones malignas y benignas tiene la mayor importancia para los dermatopatólogos debido a la consiguiente divergencia en las decisiones terapéuticas. En este contexto, un estudio utilizó una muestra de 695 neoplasias melanocíticas para distinguir entre melanoma y nevo mediante clasificación [ 105 ]. El estudio incluyó una representación completa de todas las etapas del melanoma, así como de varios tipos de nevos. En la presente investigación, se observó que la red neuronal convolucional exhibió una superioridad estadísticamente significativa sobre los patólogos en términos de diagnosticar con precisión nevos y melanoma mediante análisis histopatológico. Se encontró que la tasa de discordancia observada del 25 al 26% entre los dermatopatólogos era comparable a la similitud antes mencionada.En otro estudio de investigación, el objetivo fue evaluar la precisión de un algoritmo DL en el diagnóstico de tres afecciones dermatopatológicas mediante la utilización de imágenes de portaobjetos completos [ 106 ]. Los hallazgos del estudio indicaron que el sistema de IA demostró una alta precisión al clasificar correctamente varios tipos de carcinomas. En contraste con la sencilla clasificación binaria involucrada en el diagnóstico del melanoma y su distinción de los nevos pigmentados, el diagnóstico de los cánceres de piel no melanoma presenta una tarea más desafiante. Este desafío surge de la intrincada categorización de estas condiciones y la inclusión de diversas enfermedades benignas y malignas, junto con dermatosis inflamatorias, dentro de los diagnósticos diferenciales. Se realizó un estudio para evaluar la eficacia de las redes neuronales convolucionales para detectar y diagnosticar con precisión lesiones no pigmentadas [ 107 ].
Los hallazgos se compararon con los diagnósticos realizados por una cohorte de 95 médicos, que incluían a 62 dermatólogos con las calificaciones adecuadas. Las redes neuronales convolucionales no mostraron una precisión superior en el diagnóstico de afecciones médicas en comparación con los expertos humanos. Sin embargo, demostraron una mayor precisión en el diagnóstico de cánceres de piel prevalentes. Por el contrario, las redes neuronales convolucionales mostraron una precisión menor que los médicos en el diagnóstico de neoplasias malignas no pigmentadas poco comunes, específicamente el melanoma amelanótico.
3.10. Ortopedía
El ML supervisado se puede aplicar para clasificar a los individuos en fenotipos de dolor según la resonancia magnética cerebral, considerando la alta prevalencia de dolor prolongado en el Reino Unido, estimada entre el 30% y el 50% [ 108 ]. La ausencia de una patología tisular que corresponda al dolor, así como la dependencia de medidas autoinformadas para la clasificación de subgrupos, plantean un desafío importante a la hora de identificar los correlatos neuronales del dolor y proporcionan una descripción general completa de las aplicaciones de aprendizaje automático utilizadas en el contexto del dolor crónico. , que abarca condiciones de dolor más allá de los trastornos musculoesqueléticos [ 109 ]. Los autores destacan específicamente el uso de técnicas de aprendizaje automático para clasificar a los individuos en distintos fenotipos de dolor basándose en modelos predictivos.
Otro estudio estableció una correlación entre la biomecánica de la rodilla en el plano frontal y la capacidad de predecir el riesgo de lesiones de rodilla [ 110 ]. En este estudio, se utilizaron datos de sensores inerciales para categorizar el rendimiento de sentadillas con una sola pierna según la extensión del valgo de la rodilla [ 111 ]. La muestra del estudio estuvo compuesta por 14 participantes y se analizaron un total de 140 imágenes. Además, los investigadores buscaron las opiniones de tres evaluadores expertos sobre el riesgo potencial asociado con los desempeños observados. Se aplicó el aprendizaje supervisado para realizar la clasificación entre tres clases distintas, a saber, «pobre», «moderado» y «bueno». Los hallazgos del estudio indican que se observó que los niveles de precisión eran significativamente altos al realizar una tarea de clasificación de 2 clases. Sin embargo, cuando la complejidad de la tarea de clasificación se incrementó a una clasificación de 3 clases, los niveles de precisión experimentaron una reducción notable de aproximadamente el 30%. Hay pocos casos en los que se hayan utilizado técnicas de aprendizaje no supervisadas en el ámbito de la investigación musculoesquelética. Según un estudio, el desafío del dolor crónico evalúa la probabilidad de dolor crónico en función de los pesos asignados para diversos comportamientos de salud [ 112 ]. El estudio incluyó métodos supervisados y no supervisados para demostrar la predicción precisa de los niveles de dolor, medidos por la escala analógica visual y el índice de discapacidad de Oswestry. Estas predicciones se realizan en base a las puntuaciones correspondientes a depresión, nutrición y actividad física. Sin embargo, aunque esto enfatiza el potencial del ML para categorizar el riesgo de cronicidad utilizando datos informados por los pacientes, no se ha confirmado la efectividad del aprendizaje no supervisado por sí solo.
3.11. Neurología
La neuroimagen desempeña un papel fundamental en la práctica clínica y la investigación científica, facilitando el examen del cerebro en diversos estados de bienestar y patología. Al igual que en muchos otros dominios, la neuroimagen se mejora mediante la utilización de metodologías de análisis sofisticadas para aprovechar los datos de las imágenes de manera efectiva para investigar el cerebro y su funcionalidad. En los últimos tiempos, ML ha hecho contribuciones significativas. Además, ha desempeñado un papel crucial en la pronta identificación de afecciones agudas como el accidente cerebrovascular y en el seguimiento de los cambios en las imágenes a lo largo del tiempo. A medida que nuestra capacidad para visualizar y examinar el cerebro progresa, también lo hace nuestra comprensión de sus complejas interconexiones y su importancia a la hora de tomar decisiones terapéuticas.A pesar de encontrarse en las primeras etapas de desarrollo, la utilización de la IA en neurooncología presenta un potencial considerable. Es muy probable que los algoritmos de IA mejoren nuestra comprensión de los tumores cerebrales y desempeñen un papel fundamental en el fomento de avances en el campo de la neurooncología. El campo de la neurooncología ha experimentado un énfasis creciente en la integración de marcadores moleculares con el fin de guiar las intervenciones terapéuticas [ 113 ]. Los algoritmos de IA han demostrado una eficacia notable en la identificación no invasiva de marcadores moleculares importantes a partir de imágenes de diagnóstico, mostrando una precisión notable. En varios conjuntos de datos institucionales, los algoritmos de IA han determinado con éxito el estado mutacional de varios marcadores [ 114 , 115 ]. Además, se ha demostrado que los algoritmos basados en IA pueden identificar eficazmente marcadores moleculares en investigación, incluso en cohortes más pequeñas de pacientes [ 116 ].La utilización de IA para el análisis de diagnóstico por imágenes ha demostrado ser beneficiosa en el tratamiento clínico de los tumores cerebrales. La utilización de la IA para automatizar tareas que requieren mucha mano de obra tiene un gran potencial en el campo de la neurooncología. Múltiples estudios han demostrado la eficacia de las técnicas de DL para identificar metástasis cerebrales que miden en el rango milimétrico mediante imágenes de resonancia magnética. Además, se ha observado que modelos DL comparables han demostrado una eficacia significativa en la segmentación automatizada de tumores, mejorando así la eficiencia de la planificación del tratamiento con radioterapia [ 117 , 118 , 119 ]. La IA ha demostrado potencial para diferenciar con precisión varias neoplasias malignas del sistema nervioso central sin la necesidad de procedimientos invasivos, logrando resultados comparables a los de neurorradiólogos expertos [ 120 , 121 ]. La aplicación extensiva de estos algoritmos de IA podría resultar muy beneficiosa en entornos con recursos limitados y sin acceso a neurorradiólogos especializados.
3.12. Ginecología
A pesar de encontrar varios obstáculos, la integración de la IA en obstetricia y ginecología ha mostrado avances notables. La utilización de la IA en diversos ámbitos ha demostrado ser muy eficaz para abordar problemas persistentes relacionados con el diagnóstico y el tratamiento. Según un estudio, la IA tiene el potencial de mejorar el conocimiento y brindar asistencia a los profesionales médicos en los campos de ginecología y obstetricia [ 122 ].
Las últimas aplicaciones de los modelos de IA en ginecología implican la identificación del carcinoma de endometrio, la fertilización in vitro, el sarcoma uterino, la neoplasia intraepitelial cervical y el avance de la medicación contra el cáncer [ 123 , 124 ].
La integración de la tecnología de IA en la ultrasonografía tiene la capacidad de mejorar la adopción de la ecografía médica en diversos entornos clínicos, facilitando su aplicación más amplia por parte de los profesionales de la salud. Por lo tanto, la utilización de la IA en el campo de la ecografía para la atención prenatal tiene el potencial de ayudar a los profesionales médicos a priorizar de manera eficiente y diagnosticar con precisión las estructuras anatómicas de las personas embarazadas. En determinadas aplicaciones médicas, como la ecografía pélvica obstétrica y la ecocardiografía, donde el análisis y la medición visuales desempeñan un papel crucial, la utilización de videoclips puede proporcionar un conjunto completo de datos estructurados. Esto permite el análisis espaciotemporal y mejora las ventajas de las RNA [ 125 ]. Un estudio investigó la eficacia de los algoritmos de IA en el diagnóstico ultrasónico de pacientes embarazadas con tumores cerebrales. Se centraron específicamente en evaluar la tasa de precisión de este enfoque de diagnóstico [ 126 ]. La precisión diagnóstica lograda mediante la utilización de IA se registró en un 94,50%. Se realizó otra investigación, que tuvo un enfoque prospectivo y descriptivo. El estudio se centró en una muestra de aproximadamente 244 mujeres embarazadas en su primer trimestre de embarazo. A las participantes femeninas registradas se les preguntó específicamente sobre su utilización de hierro, ácido fólico, yoduro de potasio y suplementos multivitamínicos durante el embarazo. La utilización de un modelo ANN que incorpora variables relacionadas con controles de embarazo, ingesta de sal yodada, suplementos yodados y alimentos ricos en yodo puede usarse para predecir la deficiencia de yodo durante las primeras etapas del embarazo. Este modelo predictivo puede ayudar a los expertos a realizar un diagnóstico más factible [ 127 ]. En su estudio, Sakai et al. utilizó una representación de diagrama gráfico explicable basada en DL recientemente desarrollada para ayudar en la detección de ultrasonido cardíaco fetal. Se sabe que este proceso de detección tiene una tasa relativamente baja de detección de cardiopatías congénitas durante las etapas del segundo trimestre, principalmente debido a los desafíos asociados con el dominio de la técnica [ 128 ]. En consecuencia, la utilización de la IA en el segundo y tercer trimestre del embarazo con fines de diagnóstico, específicamente mediante la representación de diagramas, mejora el rendimiento de la detección. La tasa de precisión para los expertos aumenta del 96% al 97,50%, mientras que los no expertos mejoran del 82% al 89% [ 129 ].
3.13. Oftalmología
La utilización de la IA en el diagnóstico y tratamiento de enfermedades oculares se ha vuelto cada vez más popular debido a los hallazgos de la investigación que enfatizan su potencial para mejorar la medicina personalizada y los resultados de la atención médica [ 130 ]. Actualmente se están desarrollando numerosos algoritmos de IA para el tratamiento de pacientes diagnosticados con diabetes mellitus [ 131 ].Debido a los avances en el tratamiento de la diabetes mellitus, ha habido una mejora en el seguimiento de los pacientes, lo que ha resultado en una mayor incidencia de retinopatía diabética y edema macular diabético. La causa principal de discapacidad visual significativa y ceguera entre las personas en edad laboral es la presencia de edema macular diabético que no ha sido diagnosticado ni tratado [ 132 ]. Por lo tanto, es imperativo realizar pruebas exhaustivas de detección de retinopatía diabética a gran escala para identificar alteraciones potencialmente perjudiciales en una fase temprana, facilitando así estrategias efectivas de manejo y tratamiento. Teniendo en cuenta los patrones predominantes de crecimiento demográfico y la incidencia significativa de retinopatía diabética y edema macular diabético dentro de la comunidad, es inevitable que la detección y el diagnóstico automatizados sean cada vez más prevalentes en los entornos de atención médica oftálmica. Se han realizado esfuerzos para explorar técnicas automatizadas de detección de retina para el diagnóstico de la retinopatía diabética con el fin de mejorar el tratamiento de los pacientes y mitigar el impacto social. Se han utilizado diversas metodologías de IA, ML y DL para el diagnóstico y la clasificación automatizados de la retinopatía diabética. Los sistemas automatizados más eficaces se han desarrollado basándose en investigaciones exhaustivas realizadas en los últimos tres años. Investigaciones recientes sobre la retinopatía diabética han demostrado que las técnicas de IA han mostrado una precisión, sensibilidad y especificidad significativas en la identificación y el diagnóstico de la retinopatía diabética [ 133 ].Los sistemas de aplicación automatizados tienen el potencial de mejorar la comprensión de los médicos sobre las predicciones de la retinopatía diabética y mejorar la practicidad de los modelos de diagnóstico inteligentes en entornos clínicos del mundo real [ 133 ]. Con base en los estudios antes mencionados, se observó que el análisis automatizado de imágenes de retina exhibió un alto nivel de precisión, validez, sensibilidad y especificidad en la detección de la retinopatía diabética. Además, el rendimiento diagnóstico de las técnicas de IA se consideró clínicamente aceptable y demostró una alta reproducibilidad cuando se aplicaron al conjunto de datos de validación.La degeneración macular relacionada con la edad es una afección ocular crónica que se reconoce como un factor importante que contribuye a la discapacidad visual [ 134 ]. Pronósticos Los algoritmos de IA existen para generar predicciones personalizadas en la degeneración macular relacionada con la edad. Estos algoritmos pueden hacer predicciones sobre la presencia de drusas debajo de la retina en personas con degeneración macular relacionada con la edad. Los algoritmos de IA ofrecen capacidades de detección automatizadas para identificar drusas, fluidos y atrofia geográfica en relación con lesiones de degeneración macular relacionada con la edad. Estos algoritmos aprovechan las imágenes del fondo de ojo y el tomógrafo de coherencia óptica de dominio espectral para mejorar el diagnóstico y el tratamiento [ 135 ].
La utilización de IA en la detección automatizada de drusas es prometedora para mejorar las capacidades de diagnóstico de los oftalmólogos en la evaluación temprana y eficiente de las imágenes del fondo de ojo [ 136 ]. Se ha explorado ampliamente la aplicación de técnicas de IA en el diagnóstico y clasificación de la degeneración macular relacionada con la edad. Estudios recientes han demostrado que estos enfoques automatizados exhiben una eficacia notable, demostrando altos niveles de precisión, sensibilidad y especificidad en la detección de la degeneración macular relacionada con la edad [ 137 ].
El glaucoma, que se sitúa como el segundo factor más frecuente de discapacidad visual a escala mundial, se caracteriza por la degeneración gradual de las células ganglionares de la retina y el agotamiento permanente de los axones del nervio óptico. La identificación y el tratamiento oportunos del glaucoma son de suma importancia en la prevención de la discapacidad visual prevenible. Las técnicas de IA han demostrado una eficacia excepcional a la hora de clasificar eficazmente ojos glaucomatosos y sanos. Los oftalmólogos tienen la capacidad de utilizar estos resultados automatizados como punto de referencia, lo que les permite mejorar su proceso de toma de decisiones dentro de la práctica clínica. La utilización de aplicaciones automatizadas de IA ha demostrado una eficacia significativa y es prometedora para abordar el inminente desafío de la retinopatía diabética, la degeneración macular relacionada con la edad y las pruebas de detección de glaucoma tanto en países desarrollados como en desarrollo [ 138 ].
3.14. Pediatría
Las técnicas de imagen desempeñan un papel fundamental en el tratamiento de afecciones neurológicas, neuroquirúrgicas y neurooncológicas pediátricas [ 139 ]. Las técnicas de resonancia magnética multiparamétrica están ganando popularidad, particularmente cuando se combinan con análisis radiogenómicos que establecen conexiones entre las características de las imágenes y los biomarcadores moleculares asociados con las enfermedades. Sin embargo, incorporar este enfoque en la práctica clínica habitual sigue siendo un desafío. Las técnicas de IA pueden modelar amplios conjuntos de datos relacionados con enfermedades neurológicas infantiles, incluidos datos radiológicos, biológicos y clínicos. Esta capacidad permite la integración de dicha información en sistemas de modelado de pronóstico en una etapa temprana. En consecuencia, las técnicas de IA ofrecen una solución viable para abordar este problema [ 139 ].En determinadas aplicaciones dentro del campo de la neurorradiología pediátrica, las RNA han demostrado una eficacia notable de forma específica. Este concepto se demuestra más eficazmente mediante la utilización de la determinación del tamaño ventricular para clasificar a los niños en un grupo normal o hidrocefálico. En un estudio reciente, se realizó un análisis de la hidrocefalia y los controles [ 140 ]. Lograron una puntuación de precisión del 94,6 % para la hidrocefalia y del 85,6 % para los controles utilizando un conjunto de entrenamiento de imágenes de resonancia magnética ponderadas en T2 de alrededor de 399 niños. Estudios anteriores han informado de logros comparables en el campo de la hidrocefalia pediátrica mediante la implementación de modificaciones evolutivas en las metodologías ANN [ 141 ].
La aplicación de una máquina de vectores de soporte para la categorización de niños en grupos de lesión cerebral normal o hipóxico-isquémica, basada en la medición del ancho del cuerpo calloso, arrojó una precisión de clasificación del 95% [ 142 ]. Otro estudio utilizó una metodología comparable para examinar a un grupo de adolescentes que habían sufrido una lesión cerebral traumática. Específicamente, utilizaron imágenes de densidad de borde y máquinas de vectores de soporte para clasificar a los participantes en dos categorías: lesión cerebral traumática normal y leve [ 143 ]. El método antes mencionado, que logró una tasa de precisión del 94%, demostró un rendimiento superior en comparación con las pruebas neurocognitivas en este aspecto [ 25 ]. Las máquinas de vectores de soporte han demostrado una clasificación exitosa de diversas anomalías de las imágenes por resonancia magnética en el cerebro fetal. Estas anomalías abarcan la conectividad funcional, la madurez cerebral y anomalías fetales graves. Las precisiones de clasificación logradas por las máquinas de vectores de soporte en estos estudios oscilan entre el 79% y el 84% [ 144 ].Se han utilizado máquinas de vectores de soporte (SVM) en el análisis de textura de imágenes por resonancia magnética para examinar tumores cerebrales. Esta aplicación de aprendizaje automático tiene como objetivo analizar cuantitativamente datos de imágenes para generar una textura de imagen que generalmente es imperceptible para la percepción visual humana [ 145 ]. El análisis de textura en la práctica clínica es ventajoso para los médicos porque puede incorporar datos de imágenes completos de todo el tumor. Este enfoque tiene en cuenta la presencia de heterogeneidad intratumoral, que puede no estar representada adecuadamente por un único sitio de biopsia o incluso por múltiples sitios de biopsia [ 145 ].Un estudio amplió la aplicación del análisis de textura integrando tanto el análisis discriminante lineal como una red neuronal probabilística [ 146 ]. Su objetivo fue categorizar los tumores de la fosa posterior, específicamente el meduloblastoma, el astrocitoma pilocítico y el ependimoma. Las técnicas combinadas lograron una precisión que oscilaba entre el 86% y el 93% mediante un proceso de validación. La utilización de la IA en el diagnóstico ofrece una mejora potencial de la eficacia de los diagnósticos.Los árboles de decisión también se han utilizado en otra capacidad importante dentro del campo del ML en el contexto de la neuroimagen pediátrica. Específicamente, se han utilizado con fines de análisis de datos para proporcionar conocimientos e información sobre neuroimagen en ensayos clínicos. Se puede observar un ejemplo en un estudio en el que se utilizó un clasificador de árbol de decisión en un ensayo controlado aleatorio realizado en niños diagnosticados con autismo que estaban en tratamiento con simvastatina [ 147 ]. El estudio utilizó un clasificador forestal aleatorio para categorizar eficazmente a los niños del grupo de control que se habían sometido a tratamiento con simvastatina [ 147 ]. El clasificador logró una precisión de clasificación del 79%. Esta observación sugiere los beneficios potenciales que tales aplicaciones pueden ofrecer en el futuro.
3.15. Hematología
La IA se ha utilizado para examinar varios tipos de datos médicos, incluidos datos hematopatológicos, radiográficos, de laboratorio, genómicos, farmacológicos y químicos. El propósito de utilizar la IA en estos análisis es mejorar la precisión y eficacia del diagnóstico, la predicción de resultados y la planificación del tratamiento y ampliar nuestra comprensión de la hematología benigna y maligna. Los avances recientes en los modelos basados en CNN han demostrado la capacidad de diferenciar eficazmente entre varios tipos de leucocitos en frotis periféricos, lo que indica su potencial para automatizar las prácticas patológicas de rutina [ 148 ]. Se están realizando investigaciones en curso en el campo de la interpretación automatizada de muestras de médula ósea [ 149 ]. Las CNN también han demostrado su utilidad para caracterizar variaciones cualitativas y cuantitativas dentro de linajes celulares específicos, como la morfología de los eritrocitos y las alteraciones de la textura observadas en la anemia de células falciformes [ 150 ]. Los logros antes mencionados abarcan el diagnóstico diferencial de diversas enfermedades, como lo demuestra la capacidad de los modelos para diagnosticar con precisión la leucemia mieloide aguda, distinguir entre diferentes causas de insuficiencia de la médula ósea y funcionar como una herramienta de detección de linfoma en entornos con recursos limitados [ 151 ]. .La IA se ha aplicado en varios dominios para mejorar la confiabilidad, conveniencia y eficacia de los procesos de diagnóstico. Estudios anteriores han demostrado que los métodos CNN han demostrado ser eficaces en el diagnóstico del mieloma múltiple utilizando únicamente datos de espectrometría de masas obtenidos de sangre periférica [ 152 , 153 ]. Se ha demostrado que los modelos personalizados poseen una alta capacidad de diagnóstico cuando es difícil distinguir entre condiciones desafiantes, como diferentes causas de insuficiencia de la médula ósea. Esto se logra integrando la demografía del paciente, los datos de laboratorio y la información genética fundamental. Estudios anteriores también han utilizado métodos similares para diferenciar entre leucemia periférica y linfoma [ 154 ].La tarea del pronóstico es ampliamente reconocida como un desafío, e incluso las herramientas de pronóstico clínico comúnmente utilizadas exhiben una variabilidad notable dentro de diferentes categorías de riesgo [ 155 ]. La IA, que posee capacidades avanzadas en el procesamiento de datos complejos y no lineales, promete ofrecer pronósticos más sofisticados e individualizados. Las metodologías antes mencionadas se han utilizado en el campo de la hematología benigna para mejorar la precisión de la evaluación del riesgo de trombosis del catéter central. Estas metodologías han identificado con éxito a personas con bajo riesgo de desarrollar trombosis [ 155 ]. La IA se ha utilizado para clasificar a los pacientes sometidos a trasplantes de células madre hematopoyéticas en grupos de bajo y alto riesgo de enfermedad de injerto contra huésped aguda. Esta clasificación tiene implicaciones importantes para la toma de decisiones informadas con respecto a la administración de tratamientos inmunosupresores a estos individuos [ 156 ]. También se han realizado estudios previos en el campo de los trasplantes autólogos para el mieloma múltiple. La IA se ha utilizado en el campo de la hematología maligna para mejorar la evaluación inicial de la estratificación del riesgo de leucemia mieloide aguda y síndromes mielodisplásicos [ 157 , 158 ]. En escenarios posteriores al tratamiento, donde la enfermedad residual mínima se considera un factor de pronóstico negativo, la IA ha demostrado la capacidad de alcanzar un rendimiento comparable al de los humanos. Este logro tiene el potencial de simplificar y establecer un enfoque consistente para el manejo y análisis de este tipo de datos [ 159 ].
3.16. Unidad de Cuidados Intensivos
Los modelos de ML se han aplicado en el entorno de la unidad de cuidados intensivos (UCI) para anticipar patologías como la lesión renal aguda, identificar síntomas como el delirio y sugerir intervenciones terapéuticas adecuadas, como vasopresores y administración de líquidos en casos de sepsis. La identificación y el tratamiento oportunos de la sepsis son de suma importancia debido a su potencial para disminuir significativamente las tasas de mortalidad. Aunque el tratamiento de la sepsis temprana implica el control de la fuente y la administración de antibióticos de amplio espectro, la detección de la sepsis durante esta fase de la enfermedad plantea desafíos considerables [ 159 ]. Identificar la sepsis se vuelve cada vez más factible a medida que avanza la afección, mientras que el tratamiento plantea desafíos considerables. Debido a la naturaleza diversa de la sepsis, los métodos de diagnóstico y pronóstico existentes plantean un desafío importante en la detección temprana de la sepsis y la estimación precisa del pronóstico. Esta dificultad complica aún más la determinación de una estrategia de tratamiento adecuada para cada paciente [ 160 ]. Los modelos de predicción de IA tienen el potencial de proporcionar un valor significativo para los pacientes diagnosticados con sepsis. Los modelos de IA poseen la capacidad de mejorar la identificación oportuna de personas que requieren tratamiento con antibióticos. Ciertos modelos de predicción de IA parecen superar a los métodos de diagnóstico existentes; sin embargo, estos modelos presentan limitaciones notables, como la inclusión de variables predictivas como la presión arterial en la definición actual de sepsis. En este contexto, la evaluación del rendimiento de los modelos de IA es exagerada. Estos modelos exhiben una generalización limitada. La existencia de preocupaciones no resueltas ha resultado en una disparidad significativa entre el avance de los algoritmos y su implementación práctica en entornos clínicos. La creciente utilización de registros médicos electrónicos dentro de la UCI está impulsando la difusión de la ciencia de datos y las técnicas de aprendizaje automático en el entorno de cuidados críticos. Los datos hemodinámicos derivados de monitores, los datos de infusión obtenidos de bombas de infusión y los datos respiratorios recopilados de ventiladores generan volúmenes de datos sustanciales. Estos conjuntos de datos se pueden comparar con otras fuentes de big data, como los datos ómicos que abarcan la genómica o la proteómica. Un estudio ideó un modelo computacional que utiliza técnicas de aprendizaje por refuerzo para proponer estrategias de tratamiento óptimas de forma dinámica para pacientes adultos en la UCI [ 161 ]. Se realizó un estudio en el que se aplicaron técnicas de ML y monitorización generalizada para evaluar continuamente el delirio y la agitación en una cohorte de 22 pacientes ingresados en una UCI [ 162 ]. Los pacientes fueron categorizados según el Método de Evaluación de la Confusión para la escala ICU. Los investigadores utilizaron cámaras y acelerómetros para capturar y documentar expresiones y movimientos faciales. Se colocaron estratégicamente tres acelerómetros en la muñeca, el tobillo y el brazo del paciente para discernir y clasificar su postura. Los investigadores aplicaron un modelo de red neuronal preexistente para realizar reconocimiento facial y detectar expresiones faciales utilizando rasgos faciales individuales.
3.17. Métodos de diagnóstico
La IA tiene la capacidad de transformar fundamentalmente las metodologías aplicadas en el diagnóstico y tratamiento de enfermedades. Mediante el examen de los datos del paciente, incluidos el historial médico, los síntomas y los resultados de las pruebas, los algoritmos de IA pueden proporcionar a los médicos diagnósticos más precisos y personalizados para cada paciente. Esto tiene el potencial de facilitar la identificación de enfermedades en una etapa más temprana y mejorar la eficacia de las estrategias de tratamiento. Además, la IA puede ayudar a identificar posibles interacciones farmacológicas y reacciones adversas, garantizando que los pacientes reciban los tratamientos más seguros y eficaces.El ultrasonido (EE. UU.) ha obtenido una adopción global generalizada como modalidad de imagen primaria en varios dominios clínicos, debido a los avances continuos en las tecnologías ultrasónicas y la infraestructura de salud digital establecida. El cáncer de mama es ampliamente reconocido como una forma prevalente de cáncer entre las mujeres en todo el mundo y sigue siendo el segundo factor más importante de mortalidad relacionada con el cáncer [ 163 ]. La utilización predominante de DL en la ecografía mamaria, como se observa en la literatura analizada, se refiere al diagnóstico y categorización de masas mamarias [ 164 ]. La utilización de técnicas de DL para el análisis de imágenes abdominopélvicas tiene diversas aplicaciones en los Estados Unidos. Una parte importante de estas aplicaciones se han dirigido específicamente al examen del hígado [ 165 ]. Su investigación reveló que este enfoque exhibía una precisión superior en comparación con la elastografía de ondas de corte bidimensional y ciertos biomarcadores en la evaluación de la fibrosis avanzada y la cirrosis en pacientes infectados con el virus de la hepatitis B. En un estudio, los autores idearon un enfoque CNN para predecir la puntuación METAVIR, una medida semicuantitativa de la fibrosis hepática [ 166 ]. El conjunto de datos de entrenamiento constaba de varios miles de imágenes estadounidenses obtenidas de dos centros de referencia académicos terciarios. Este enfoque demostró un nivel notable de precisión en la predicción de la puntuación METAVIR, superando las capacidades de diagnóstico de los radiólogos para identificar la fibrosis hepática. En su estudio, Ta et al. desarrolló un sistema de diagnóstico asistido por computadora para la clasificación de lesiones hepáticas focales malignas y benignas utilizando grabaciones de cine con ultrasonido con contraste [ 167 ]. Los investigadores descubrieron que la precisión de este método era comparable a la de un lector experto.
Los algoritmos de aprendizaje profundo se han utilizado en diversas aplicaciones, incluida la identificación de enfermedades musculares [ 168 ], la determinación del posicionamiento de los conos y la segmentación de imágenes musculares [ 169 ]. La precisión del diagnóstico de las enfermedades neuromusculares se mejoró mediante el uso de un método basado en CNN, que mejoró la evaluación y clasificación de las enfermedades inflamatorias de los músculos [ 168 ]. El progreso en el campo de las herramientas de IA/ML para la interpretación de imágenes está experimentando una rápida aceleración. Esto puede atribuirse a varios factores, incluida la disponibilidad de amplios conjuntos de datos de imágenes digitalizadas, la accesibilidad de algoritmos de código abierto, los avances en la potencia informática, la aparición de servicios en la nube y el desarrollo continuo de técnicas de DL [ 170 ].La utilización de la automatización en tareas frecuentemente realizadas por radiólogos, como identificar fracturas costales y nódulos pulmonares mediante tomografías computarizadas, reevaluar el tamaño del derrame pleural mediante radiografías de tórax secuenciales o realizar exámenes mamográficos, muestra potencial como una estrategia favorable. Esto tiene el potencial de permitir a los radiólogos dedicar tiempo adicional a tareas interpretativas más avanzadas que pueden no ser susceptibles de automatización, así como participar en esfuerzos como reuniones de equipos multidisciplinarios. La utilización de IA en el procedimiento de clasificación demuestra una capacidad notable para asignar prioridad de manera eficiente a casos críticos que requieren notificación inmediata. Estos casos pueden incluir tomografías computarizadas que revelan la presencia de embolia pulmonar, radiografías de tórax que indican neumotórax o tomografías computarizadas de la cabeza que revelan hemorragia. La metodología antes mencionada posee la capacidad de reducir la morbilidad de los pacientes y acelerar la duración de la hospitalización en los servicios de urgencias. La utilización de sistemas DL en resonancia magnética sintética permite el posprocesamiento y la reconstrucción de datos de imágenes de resonancia magnética, lo que reduce el tiempo de adquisición de imágenes sin un deterioro significativo en la calidad de la imagen. Este avance puede potencialmente mejorar la eficiencia, disminuir los gastos y mejorar la accesibilidad [ 171 ].Las CNN son un elemento fundamental dentro de las redes utilizadas en radiología ortopédica y musculoesquelética [ 172 ]. En los últimos tiempos se ha introducido el concepto de redes generativas adversarias (GAN). Las GAN son modelos diseñados para generar datos novedosos que se parecen mucho al conjunto de datos original. Estos modelos comprenden dos redes distintas que participan en un proceso de entrenamiento competitivo similar a un juego. Se han utilizado con éxito un total de 12 modelos GAN mejorados que incorporan CNN en el dominio de las imágenes radiográficas [ 173 ].Se han realizado amplias investigaciones en el campo de la radiología oral y maxilofacial para investigar el potencial de la IA en el diagnóstico de diversas afecciones. Las condiciones antes mencionadas abarcan caries dental, enfermedad periodontal, osteosclerosis, quistes odontogénicos y tumores, así como dolencias que impactan el seno maxilar o las articulaciones temporo mandibulares. La IA se ha utilizado en el campo de la odontología para el análisis de imágenes, abarcando una variedad de tareas, incluida la segmentación y localización de los dientes, la evaluación de la calidad ósea para la osteoporosis, la determinación de la edad ósea mediante radiografías de mano y muñeca y la localización de puntos de referencia cefalométricos [ 172 ]. . Los sistemas DL que utilizan arquitecturas CNN se han aplicado con éxito en el ámbito de la odontología. En particular, se ha desarrollado un novedoso sistema que incorpora imágenes de tomografía computarizada de haz cónico tridimensionales e imágenes bidimensionales [ 172 ].La aplicación de técnicas de DL se ha utilizado para identificar y categorizar dientes tanto en imágenes de tomografía computarizada de haz cónico como en imágenes panorámicas. La utilización de sistemas de clasificación de dientes permite a los dentistas tomar decisiones clínicas y optimizar su proceso de gráficos mediante el uso de resultados de diseño automatizados asistidos por computadora. Estos resultados facilitan la finalización automática de los registros digitales de los pacientes [ 174 ].
4. Discusión
4.1. General
El objetivo de esta revisión de la literatura es proporcionar una descripción general completa de la investigación existente sobre la IA en la práctica clínica. Además de su amplio uso en técnicas de diagnóstico, la integración de la IA se ha explorado en diversas disciplinas médicas, incluidas cardiología, anestesiología, cirugía, neumología, neurología, urología, ginecología, hematología y pediatría. Dada la afluencia continua de nuevos artículos y el aumento exponencial de los artículos publicados, esta revisión se centra en artículos indicativos para ilustrar la sólida penetración y las amplias aplicaciones de la IA en la práctica clínica.Una de las principales ventajas de la IA en la práctica clínica es su capacidad para mejorar la precisión del diagnóstico y los resultados del tratamiento [ 10 , 11 , 12 , 13 , 14 , 15 , 16 , 17 , 18 , 19 , 20 , 21 , 22 ]. Con algoritmos impulsados por IA, los proveedores de atención médica pueden analizar grandes cantidades de datos de pacientes e identificar patrones que pueden no ser inmediatamente evidentes para los médicos humanos. Esto puede ayudar a identificar enfermedades antes, lo que resulta en una intervención médica acelerada y mejores pronósticos para las personas. Además, la IA puede predecir qué tratamientos probablemente sean más efectivos para un paciente determinado, lo que permite una medicina personalizada que considera las características individuales del paciente. La IA puede ayudar a reducir los costos de atención médica al agilizar los procesos administrativos y reducir las pruebas innecesarias [ 23 ].En un estudio, se aplicaron técnicas de aprendizaje automático en el análisis de datos de secuenciación del genoma de alto rendimiento, con el objetivo de mejorar la comprensión de los procesos patológicos y el desarrollo de modalidades terapéuticas [ 175 ]. En este estudio, se aplicaron algoritmos de aprendizaje automático de vanguardia, incluido el bosque aleatorio, el núcleo radial de la máquina de vectores de soporte, el impulso adaptativo, la red neuronal promediada y la máquina de impulso de gradiente. El objetivo era estratificar a los pacientes con carcinoma de células escamosas de cabeza y cuello en estadios clínicos tempranos y tardíos y predecir el riesgo en función de los perfiles de expresión de los miARN [ 175 ]. Además, muy recientemente, se introdujeron codificadores automáticos variacionales (es decir, un tipo de red neuronal) como un método para aumentar eficazmente el tamaño de la muestra de los estudios clínicos, mitigando así los costos, las limitaciones de tiempo, los abandonos y las consideraciones éticas [ 176 ]. En un estudio, la eficacia de los codificadores automáticos variacionales en el contexto del aumento de datos se demostró mediante la utilización de simulaciones que abarcan múltiples escenarios [ 176 ]. Además, en el campo de los estudios de bioequivalencia, se utilizaron varios métodos de ML para resolver el antiguo problema de definir la métrica de tasa de absorción adecuada [
20 ,
21 ,
22 ]. Mediante la utilización conjunta de algoritmos de ML, modelos de efectos mixtos no lineales y simulaciones de Monte Carlo, se definió e introdujo una nueva métrica denominada «pendiente promedio». Se demostró que la Cmax actualmente utilizada (es decir, la concentración plasmática máxima observada) no es adecuada para expresar la tasa de absorción. Por el contrario, la medida recién definida (pendiente promedio) comprende las propiedades deseadas de la tasa de absorción, tiene las unidades de medida apropiadas (es decir, unidades de concentración por tiempo), muestra facilidad de estimación directamente a partir de los datos de concentración-tiempo del fármaco, y todos los algoritmos de ML mostraron su supremacía sobre todas las demás métricas utilizadas o propuestas en bioequivalencia [ 20 , 21 , 22 ].Aunque las ventajas de la IA en la práctica clínica son evidentes, existen una serie de obstáculos que requieren atención y resolución [ 177 ]. Una de las consideraciones más importantes gira en torno a la posibilidad de que la IA mantenga y propague prejuicios dentro del sector de la salud. Si los algoritmos utilizados en los sistemas de IA se basan en datos sesgados, pueden producir resultados sesgados, lo que genera disparidades en los resultados de atención médica para ciertas poblaciones de pacientes. Además, existe una falta de transparencia, interpretabilidad y explicabilidad de los algoritmos de IA, ya que estos últimos pueden considerarse como una caja negra. Esta cuestión se discutirá más adelante. Además, existe el riesgo de que la IA pueda deshumanizar la atención médica, haciendo que los pacientes se sientan desconectados de sus proveedores de atención y reducidos a un conjunto de puntos de datos. También existen temores sobre las implicaciones éticas del uso de la IA en la atención sanitaria, en particular. El impacto de la integración de las tecnologías de IA en el campo de la medicina será más pronunciado entre los médicos actuales y futuros. En consecuencia, es imperativo que las facultades de medicina y los programas de educación médica de posgrado modifiquen su plan de estudios para instruir a las generaciones actuales y futuras de médicos sobre la utilización consciente de estas tecnologías potentes y transformadoras [ 178 ]. La integración de la IA en la medicina introduce varias consideraciones legales y éticas, incluidas cuestiones de responsabilidad médica, como la capacitación y la competencia, la transparencia/trazabilidad, la explicabilidad, los datos personales de salud, el cumplimiento normativo, la responsabilidad del producto y el seguro por negligencia. Los aspectos fundamentales de estas cuestiones se detallan a continuación.
4.2. Formación de profesionales sanitarios
Los profesionales sanitarios que utilizan sistemas de IA necesitan una formación adecuada para garantizar la competencia en su uso. No comprender y operar adecuadamente los sistemas de IA puede provocar errores médicos y responsabilidad posterior. Además, los futuros estudiantes de medicina deberán desarrollar nuevas habilidades, que abarquen el concepto de “captura de conocimientos, no retención de conocimientos”. Esto implica un cambio de un plan de estudios centrado en la memorización a uno que priorice el pensamiento crítico. El campo de la IA pone un énfasis significativo en dos dominios principales: la colaboración y la gestión de aplicaciones de IA, así como una comprensión más profunda de las probabilidades y su consiguiente aplicación en la toma de decisiones clínicas que involucran a pacientes y familias. Los dominios antes mencionados tienen como objetivo adquirir conocimientos relacionados con la utilización eficiente y ética de la IA, al mismo tiempo que promueven la aplicación práctica de las tecnologías de IA en el campo de la salud [ 179 ].
4.3. Transparencia, Trazabilidad y Explicabilidad
Inspirándose en diversas disciplinas, los ámbitos de transparencia y trazabilidad en el contexto de la atención sanitaria y de los pacientes individuales requieren el cumplimiento de criterios más rigurosos [ 180 ]. Desde un punto de vista legal, es necesario que los datos cumplan con todas las leyes, regulaciones y obligaciones legales adicionales aplicables durante todo su ciclo de vida, incluida la adquisición, el almacenamiento, la transferencia, el procesamiento y el análisis. Además, es imperativo que la ley, su interpretación y su implementación se ajusten continuamente en respuesta a los avances tecnológicos en constante cambio [ 181 ]. Numerosos algoritmos de IA, en particular aquellos basados en modelos de aprendizaje profundo, funcionan como enigmáticas “cajas negras”, lo que dificulta aclarar el fundamento de sus decisiones. En situaciones en las que se examina la validez de una decisión médica generada por un sistema de inteligencia artificial, la falta de transparencia puede dar lugar a complicaciones legales. Incluso cuando se cumplen todos estos aparentes requisitos previos, persiste la pregunta de si la utilización de soluciones y herramientas impulsadas por la IA requiere la necesidad de explicabilidad. En esencia, los médicos y los pacientes deben poseer conocimientos sobre los resultados presentados y una comprensión de las cualidades y atributos en los que se basan estos resultados, así como los correspondientes supuestos subyacentes. Además, la inclusión de partes interesadas adicionales puede requerir una comprensión y explicación integral de algoritmos y modelos. Desde un punto de vista jurídico occidental, se han identificado tres áreas fundamentales con el fin de dilucidar el concepto de explicabilidad [ 182 ]. Estas áreas incluyen (a) consentimiento informado, (b) certificación y aprobación de acuerdo con las regulaciones establecidas por la FDA y el Reglamento de Dispositivos Médicos (MDR), y (c) Responsabilidad.
4.4. Responsabilidad y marco regulatorio
Los organismos de certificación y aprobación responsables de los dispositivos médicos han sido relativamente lentos en la implementación de regulaciones relacionadas con la IA explicable y su impacto en el desarrollo y comercialización de dichos productos. La FDA promueve significativamente el desarrollo y la mejora continuos de productos médicos basados en IA a través de su enfoque integral del ciclo de vida total del producto. No se hace referencia explícita al concepto de explicabilidad; sin embargo, existe el requisito de un nivel adecuado de transparencia y claridad en el resultado y el algoritmo destinados a los usuarios [ 183 , 184 ]. El foco principal de esta investigación se refiere a las funcionalidades del software y las modificaciones que ha sufrido a lo largo de su evolución. El MDR no aborda explícitamente el requisito de explicabilidad en relación con los dispositivos médicos que utilizan IA y ML, específicamente. En este contexto, es importante enfatizar la importancia de la rendición de cuentas y la transparencia [ 185 ]. Específicamente, estos requisitos se refieren al suministro de información que permita el rastreo, la transparencia y la explicación del proceso de desarrollo de modelos de ML y DL que contribuyen al tratamiento médico. Existe una gran probabilidad de que en los próximos tiempos surja una delimitación más refinada de estos requisitos previos, lo que requerirá que los fabricantes de dispositivos/software médicos impulsados por IA proporcionen detalles exhaustivos relacionados con la capacitación y evaluación de los modelos, los datos utilizados y la metodologías generales utilizadas en su creación.La integración de la IA en la atención sanitaria implica frecuentemente la utilización de datos de pacientes altamente sensibles. Supongamos que una violación de la seguridad o la privacidad de los datos da como resultado un acceso o uso no autorizado de la información del paciente; Los proveedores de atención médica y los desarrolladores de inteligencia artificial pueden enfrentar repercusiones legales. Esto subraya la importancia crítica de medidas sólidas de protección de datos y el cumplimiento de las regulaciones de privacidad en el desarrollo e implementación de aplicaciones de IA dentro del sector de la salud [ 185 ]. El procesamiento de datos personales de salud está permitido por la ley sólo cuando el individuo ha dado su consentimiento explícito para su utilización. El estándar actual para utilizar datos de pacientes en aplicaciones de IA es el consentimiento informado, ya que falta una legislación general que regule el uso de datos e información personales [ 185 ]. Las organizaciones de atención médica y los desarrolladores de IA deben cumplir con diversas regulaciones de protección de datos, como la Ley de Responsabilidad y Portabilidad de Seguros Médicos (HIPAA) en los Estados Unidos o el Reglamento General de Protección de Datos (GDPR) en Europa [ 186 , 187 ]. El incumplimiento de estas normas puede tener consecuencias legales y multas. Se deben establecer políticas claras con respecto a la propiedad de los datos y el consentimiento del paciente. Se debe informar a los pacientes sobre cómo se utilizarán sus datos, quién tendrá acceso a ellos y con qué fines. La obtención del consentimiento informado es esencial por razones éticas y legales. La implementación de métodos de cifrado sólidos tanto para los datos en tránsito como para los datos en reposo ayuda a proteger la información del paciente contra el acceso no autorizado. El cifrado agrega una capa adicional de seguridad para evitar que partes no autorizadas intercepten o accedan a datos confidenciales. El acceso a los sistemas de inteligencia artificial de la atención médica y a los datos que procesan debe restringirse y monitorearse. Se deben implementar controles de acceso basados en roles para garantizar que solo el personal autorizado pueda acceder a información confidencial. Además, los sistemas de inteligencia artificial para el cuidado de la salud deben utilizar métodos seguros para almacenar y transmitir datos, mientras que las auditorías y evaluaciones de seguridad periódicas ayudan a identificar vulnerabilidades en el sistema.El marco legal relativo a la IA en la atención sanitaria todavía se encuentra en estado de evolución. Es posible que se introduzcan nuevas leyes y regulaciones para abordar cuestiones relacionadas específicamente con la responsabilidad, y los profesionales de la salud deben mantenerse informados sobre estos cambios. A medida que el campo de la IA continúa avanzando, es probable que los marcos legales se adapten para garantizar que se sigan prácticas éticas, transparentes y responsables en el desarrollo y la implementación de tecnologías de IA en la atención médica. Mantenerse al tanto de estas regulaciones en evolución es crucial para que los profesionales de la salud naveguen por el complejo terreno legal y defiendan los estándares de responsabilidad y atención al paciente. Sin embargo, incluso hasta el día de hoy, persisten disparidades en la orientación internacional entre Europa y Estados Unidos con respecto a los desafíos legales que pueden surgir del uso de la IA en la atención médica. Estas regiones adoptan enfoques distintos para abordar estos desafíos. La Unión Europea (UE) se ha convertido en una fuerza líder en el campo de la innovación en IA médica y ha reconocido las dificultades específicas que plantea la IA para los marcos de responsabilidad actuales. Para establecer coherencia en los principios de responsabilidad y garantizar claridad jurídica, la Comisión Europea ha introducido la Ley de Inteligencia Artificial, que representa uno de los marcos legales iniciales dedicados específicamente a la IA [ 186 ]. La Comisión Europea se esfuerza por promover la utilización segura de la IA en sectores con consecuencias importantes, como la atención sanitaria, al tiempo que mejora la innovación tecnológica. Estados Unidos carece de un marco legal integral que regule específicamente la IA, lo que resulta en un precedente legal limitado en materia de responsabilidad e IA médica. La FDA ha reconocido el aspecto regulatorio de la IA en la atención médica, cuyo objetivo es facilitar la implementación segura de la IA mediante el desarrollo de un plan estratégico para garantizar la supervisión continua de la IA como dispositivo médico [ 187 ]. Para fomentar un enfoque centrado en el paciente, la FDA se esfuerza por mejorar la transparencia solicitando a los fabricantes que proporcionen descripciones detalladas de los mecanismos operativos de sus dispositivos de IA. Esta iniciativa tiene como objetivo facilitar una comprensión integral de las ventajas y los peligros potenciales asociados con dichos dispositivos. La FDA también se esfuerza por abordar los posibles sesgos que pueden surgir del entrenamiento de algoritmos de IA en poblaciones específicas o conjuntos de datos históricos [ 187 ]. La FDA ha publicado recientemente un documento de debate titulado “Marco regulatorio propuesto para modificaciones del software basado en inteligencia artificial/aprendizaje automático como dispositivo médico” con el objetivo de garantizar la seguridad del software médico que utiliza tecnologías de inteligencia artificial y aprendizaje automático. Además, a medida que el uso de la IA en la atención sanitaria se vuelve más frecuente, las consideraciones sobre seguros contra negligencias evolucionan para abordar los riesgos potenciales asociados con estas tecnologías [ 188 ]. Dados los riesgos únicos asociados con la IA en la atención médica, es posible que sea necesario adaptar las pólizas de seguro contra negligencias para abordar las responsabilidades que surjan específicamente del uso de tecnologías de IA. Esto podría incluir cobertura por errores o mal funcionamiento en los algoritmos de IA que provoquen resultados adversos para los pacientes. Las aseguradoras pueden enfrentar desafíos al suscribir pólizas relacionadas con la IA, ya que el campo está evolucionando rápidamente y la evaluación de los riesgos asociados con las tecnologías emergentes puede ser compleja. Es posible que las aseguradoras necesiten adaptar sus procesos de suscripción para tener en cuenta los riesgos específicos que plantea la IA en la atención sanitaria [ 189 ]. Las pólizas de seguro contra negligencias relacionadas con la IA deben alinearse con los marcos legales y regulatorios en evolución que rigen el uso de la IA en la atención médica. Es posible que las aseguradoras necesiten mantenerse informadas sobre los cambios en las leyes y regulaciones para garantizar que sus políticas sigan siendo relevantes y conformes. Además, las aseguradoras pueden exigir a las organizaciones sanitarias que implementen mecanismos de seguimiento y notificación de incidentes relacionados con la IA. Informar oportunamente los eventos adversos puede facilitar una respuesta proactiva y ayudar a mitigar posibles responsabilidades. En la misma línea, la responsabilidad del producto en el contexto de la IA se refiere a la responsabilidad legal de quienes participan en el diseño, desarrollo, fabricación, distribución y despliegue de sistemas de IA por cualquier daño o daño causado por el producto de IA [ 190 , 191 ]. . Si el diseño de un sistema de IA es intrínsecamente defectuoso y tiene consecuencias perjudiciales, los diseñadores y desarrolladores pueden ser considerados responsables. Los defectos del diseño de la IA podrían incluir algoritmos sesgados, pruebas inadecuadas o falta de funciones de seguridad sólidas. Los defectos de fabricación se refieren a problemas que surgen durante la producción o implementación de un sistema de IA. Estos defectos pueden provocar fallos de funcionamiento, vulnerabilidades de seguridad u otros problemas que podrían provocar daños. Los fabricantes pueden ser considerados responsables de estos defectos. Si los productos de IA vienen con advertencias o instrucciones inadecuadas sobre su uso adecuado, es posible que los profesionales de la salud o los usuarios finales no sean conscientes de los riesgos potenciales. No proporcionar una orientación clara sobre las limitaciones y riesgos de un sistema de IA podría dar lugar a responsabilidad. En los casos en que proveedores externos proporcionen componentes o servicios de IA, la responsabilidad puede extenderse a estos proveedores si sus productos o servicios contribuyen al daño. Determinar la cadena de responsabilidad y responsabilidad en ecosistemas complejos de IA puede resultar un desafío. Las pruebas y validaciones rigurosas de los sistemas de IA son esenciales para identificar y abordar problemas potenciales antes de su implementación. Si las pruebas inadecuadas contribuyen al daño, las partes responsables del proceso de prueba y validación pueden ser consideradas responsables. Mantener registros detallados de los procesos de diseño, desarrollo, pruebas e implementación es importante para demostrar la debida diligencia en caso de un reclamo por responsabilidad del producto. La documentación clara puede proporcionar evidencia del cumplimiento de los estándares y las mejores prácticas de la industria.
4.5. En general
Esta revisión de la literatura analiza las aplicaciones actuales de la IA en diversas especialidades médicas en la práctica clínica. La IA posee la capacidad de transformar fundamentalmente la práctica clínica y mejorar los resultados de los pacientes. El potencial para futuros avances en la tecnología de IA es enorme y el impacto en los resultados de los pacientes podría ser significativo. Ciertamente, no se podrían haber incluido todos los aspectos y referencias bibliográficas, ya que esta revisión de la literatura tiene como objetivo ofrecer una visión integral de las aplicaciones de la IA en tantas especialidades médicas como sea posible. En consecuencia, era inevitable que no se pudieran discutir algunas contribuciones importantes en cada campo. A modo de ejemplo, ha habido un aumento sustancial en la utilización de biomarcadores como sistemas de alerta temprana para evaluar el riesgo de enfermedad durante la última década, con una aplicación amplia evidente durante la reciente pandemia de COVID-19 [ 192 ]. En el mismo contexto, en dermatología, que es uno de los campos con mayor uso de la IA, recientemente un artículo de investigación ha subrayado la capacidad del aprendizaje automático para servir como biomarcador para diferenciar entre individuos con psoriasis, artritis psoriásica y aquellos que gozan de buena salud [ 193 ]. Además, se han llevado a cabo varias investigaciones que han descubierto biomarcadores moleculares notables a través de la expresión de miARN que pueden diferenciar entre las etapas tempranas y tardías de los carcinomas [ 175 ].También se debe enfatizar que a pesar de las preocupaciones discutidas en esta revisión, no se pueden ignorar los beneficios potenciales de la IA en la atención médica. La IA tiene la capacidad de mejorar la precisión del diagnóstico, personalizar los planes de tratamiento y reducir los costos de atención médica. En el futuro, la IA probablemente se convertirá en una herramienta estándar en la práctica clínica, y los proveedores de atención médica trabajarán junto con los sistemas de IA para brindar la mejor atención posible a los pacientes [ 185 , 186 ]. Sin embargo, para garantizar el uso ético y eficiente de la IA en el sector sanitario, debemos afrontar estos temores y establecer protocolos explícitos para avanzar e integrar los sistemas de IA. La plena realización del potencial de la IA para mejorar los resultados de la atención sanitaria sólo puede lograrse en tales circunstancias. En general, se considera que la IA tiene potencial para mejorar en gran medida los resultados de la atención sanitaria, pero es importante abordar las preocupaciones éticas y establecer directrices claras para su desarrollo e implementación.
5. Conclusiones
La integración de la IA en la práctica clínica genera muchos beneficios y desafíos con importantes implicaciones para consideraciones éticas y legales. La IA promete mejorar la precisión del diagnóstico, simplificar las tareas administrativas y personalizar los planes de tratamiento. Al analizar grandes cantidades de datos médicos, los sistemas de inteligencia artificial pueden identificar patrones y correlaciones que podrían escapar a la observación humana, lo que conduciría a intervenciones más precisas y oportunas. Además, la IA puede contribuir a soluciones sanitarias rentables y mejorar los resultados generales de los pacientes. Esta integración de la tecnología de IA facilita los procesos de toma de decisiones clínicas informadas. Por lo tanto, la IA tiene el potencial de mejorar los resultados de los pacientes, ofreciendo diagnósticos más rápidos y precisos, planes de tratamiento personalizados y costos de atención médica reducidos. Si bien todavía queda mucho por explorar y desarrollar en el campo de la IA en la práctica clínica, es crucial que sigamos invirtiendo en investigación y desarrollo para desbloquear todo su potencial. Este enfoque puede mejorar nuestra comprensión de cómo la IA puede mejorar la atención sanitaria y conducir al desarrollo de nuevas herramientas y tecnologías que beneficien tanto a los pacientes como a los profesionales sanitarios. Sin embargo, es importante abordar su desarrollo e implementación con cautela y colaborar con los profesionales de la salud para garantizar que se cumplan las consideraciones éticas. Sin embargo, estos avances conllevan dilemas éticos y complejidades legales. El uso de la IA en la toma de decisiones clínicas genera preocupaciones sobre la transparencia, la responsabilidad y el potencial de sesgo en los algoritmos. Garantizar la privacidad del paciente y la seguridad de los datos se vuelve primordial, lo que exige directrices éticas y marcos legales sólidos. Lograr el equilibrio adecuado entre innovación y salvaguardia de los derechos de los pacientes requiere una cuidadosa consideración de las implicaciones éticas de la IA en la práctica clínica, junto con el desarrollo de marcos legales que puedan adaptarse al rápido ritmo de la evolución tecnológica en el sector de la salud. Para superar los desafíos éticos y legales asociados con la integración de la IA en la práctica clínica, es esencial un enfoque multifacético que incluya marcos y regulaciones legales, IA transparente y explicable, pautas y estándares éticos, auditorías y evaluaciones periódicas, incentivos para las prácticas éticas. y colaboración internacional.
References
- Henderson, H. Artificial Intelligence: Mirrors for the Mind (Milestones in Discovery and Invention), 1st ed.; Chelsea House Publisher:
New York, NY, USA, 2007; 176p. - Russell, S.; Norvig, P. Artificial Intelligence: A Modern Approach, 4th ed.; Pearson: Bloomington, MN, USA, 2021; 1136p.
- Philippidis, A. Charles River Licenses ERS Genomics’ CRISPR/Cas9 Technology. Clin. OMICs 2018, 5, 7. [CrossRef]
- Turing, A.M. On Computable Numbers, with an Application to the Entscheidungsproblem. Proc. Lond. Math. Soc. 1937, s2-42,
230–265. [CrossRef] - McCulloch, W.S.; Pitts, W. A Logical Calculus of the Ideas Immanent in Nervous Activity. Bull. Math. Biophys. 1943, 5, 115–133.
[CrossRef] - Widrow, B.; Lehr, M.A. 30 Years of Adaptive Neural Networks: Perceptron, Madaline, and Backpropagation. Proc. IEEE 1990,
78, 1415–1442. [CrossRef] - Lodwick, G.S.; Keats, T.E.; Dorst, J.P. The Coding of Roentgen Images for Computer Analysis as Applied to Lung Cancer. Radiology
1963, 81, 185–200. [CrossRef] [PubMed] - Feigenbaum, E.A.; Buchanan, B.G. DENDRAL and Meta-DENDRAL: Roots of Knowledge Systems and Expert System Applications. Artif. Intell. 1993, 59, 233–240. [CrossRef]
- Goldberg, J.E.; Reig, B.; Lewin, A.A.; Gao, Y.; Heacock, L.; Heller, S.L.; Moy, L. New Horizons: Artificial Intelligence for Digital
Breast Tomosynthesis. RadioGraphics 2023, 43, e220060. [CrossRef] - Zhong, F.; Xing, J.; Li, X.; Liu, X.; Fu, Z.; Xiong, Z.; Lu, D.; Wu, X.; Zhao, J.; Tan, X.; et al. Artificial Intelligence in Drug Design.
Sci. China Life Sci. 2018, 61, 1191–1204. [CrossRef] - Bakkar, N.; Kovalik, T.; Lorenzini, I.; Spangler, S.; Lacoste, A.; Sponaugle, K.; Ferrante, P.; Argentinis, E.; Sattler, R.; Bowser, R.
Artificial Intelligence in Neurodegenerative Disease Research: Use of IBM Watson to Identify Additional RNA-Binding Proteins
Altered in Amyotrophic Lateral Sclerosis. Acta Neuropathol. 2017, 135, 227–247. [CrossRef] - Segler, M.H.S.; Preuss, M.; Waller, M.P. Planning Chemical Syntheses with Deep Neural Networks and Symbolic AI. Nature 2018,
555, 604–610. [CrossRef] - Simões, M.F.; Silva, G.; Pinto, A.C.; Fonseca, M.; Silva, N.E.; Pinto, R.M.A.; Simões, S. Artificial Neural Networks Applied to
Quality-by-Design: From Formulation Development to Clinical Outcome. Eur. J. Pharm. Biopharm. 2020, 152, 282–295. [CrossRef]
[PubMed] - Gaisford, S.; Saunders, M. Essentials of Pharmaceutical Preformulation, 1st ed.; Wiley-Blackwell: Hoboken, NJ, USA, 2013; 268p.
- Babu, N.J.; Nangia, A. Solubility Advantage of Amorphous Drugs and Pharmaceutical Cocrystals. Cryst. Growth Des. 2011,
11, 2662–2679. [CrossRef] - Damiati, S.A.; Martini, L.G.; Smith, N.W.; Lawrence, M.J.; Barlow, D.J. Application of Machine Learning in Prediction of
Hydrotrope-Enhanced Solubilisation of Indomethacin. Int. J. Pharm. 2017, 530, 99–106. [CrossRef] [PubMed]
- Hossain, S.; Kabedev, A.; Parrow, A.; Bergström, C.A.S.; Larsson, P. Molecular Simulation as a Computational Pharmaceutics
Tool to Predict Drug Solubility, Solubilization Processes and Partitioning. Eur. J. Pharm. Biopharm. 2019, 137, 46–55. [CrossRef]
[PubMed] - Ye, Z.; Yang, Y.; Li, X.; Cao, D.; Ouyang, D. An Integrated Transfer Learning and Multitask Learning Approach for Pharmacokinetic
Parameter Prediction. Mol. Pharm. 2018, 16, 533–541. [CrossRef] - Ota, R.; Yamashita, F. Application of Machine Learning Techniques to the Analysis and Prediction of Drug Pharmacokinetics.
J. Control. Release 2022, 352, 961–969. [CrossRef] - Karalis, V.D. Machine Learning in Bioequivalence: Towards Identifying an Appropriate Measure of Absorption Rate. Appl. Sci.
2022, 13, 418. [CrossRef] - Karalis, V.D. On the Interplay between Machine Learning, Population Pharmacokinetics, and Bioequivalence to Introduce
Average Slope as a New Measure for Absorption Rate. Appl. Sci. 2023, 13, 2257. [CrossRef] - Karalis, V.D. An In Silico Approach toward the Appropriate Absorption Rate Metric in Bioequivalence. Pharmaceuticals 2023,
16, 725. [CrossRef] - Ferrara, P.; Battiato, S.; Polosa, R. Progress and Prospects for Artificial Intelligence in Clinical Practice: Learning from COVID-19.
Intern. Emerg. Med. 2022, 17, 1855–1857. [CrossRef] - Beneke, F.; Mackenrodt, M.-O. Artificial Intelligence and Collusion. IIC-Int. Rev. Intellect. Prop. Compet. Law 2018, 50, 109–134.
- Steels, L.; Brooks, R. The Artificial Life Route to Artificial Intelligence: Building Embodied, Situated Agents, 1st ed.; Routledge: London,
UK, 2018; 300p. - Bielecki, A. Models of Neurons and Perceptrons: Selected Problems and Challenges, 1st ed.; Springer International Publishing:
Berlin/Heidelberg, Germany, 2019; 156p. - van der Maaten, L.; Hinton, G. Visualizing Non-Metric Similarities in Multiple Maps. Mach. Learn. 2011, 87, 33–55. [CrossRef]
- Gadd, C.; Wade, S.; Shah, A.A. Pseudo-Marginal Bayesian Inference for Gaussian Process Latent Variable Models. Mach. Learn.
2021, 110, 1105–1143. [CrossRef] - Gallego, V.; Naveiro, R.; Roca, C.; Ríos Insua, D.; Campillo, N.E. AI in Drug Development: A Multidisciplinary Perspective.
Mol. Divers. 2021, 25, 1461–1479. [CrossRef] [PubMed] - Kaul, V.; Enslin, S.; Gross, S.A. History of Artificial Intelligence in Medicine. Gastrointest. Endosc. 2020, 92, 807–812. [CrossRef]
[PubMed] - Kusunose, K. Steps to Use Artificial Intelligence in Echocardiography. J. Echocardiogr. 2020, 19, 21–27. [CrossRef] [PubMed]
- Kusunose, K.; Haga, A.; Abe, T.; Sata, M. Utilization of Artificial Intelligence in Echocardiography. Circ. J. 2019, 83, 1623–1629.
[CrossRef] - Dey, D.; Slomka, P.J.; Leeson, P.; Comaniciu, D.; Shrestha, S.; Sengupta, P.P.; Marwick, T.H. Artificial Intelligence in Cardiovascular
Imaging. J. Am. Coll. Cardiol. 2019, 73, 1317–1335. [CrossRef] - van Hamersvelt, R.W.; Zreik, M.; Voskuil, M.; Viergever, M.A.; Išgum, I.; Leiner, T. Deep Learning Analysis of Left Ventricular
Myocardium in CT Angiographic Intermediate-Degree Coronary Stenosis Improves the Diagnostic Accuracy for Identification of
Functionally Significant Stenosis. Eur. Radiol. 2018, 29, 2350–2359. [CrossRef] - Zhang, N.; Yang, G.; Gao, Z.; Xu, C.; Zhang, Y.; Shi, R.; Keegan, J.; Xu, L.; Zhang, H.; Fan, Z.; et al. Deep Learning for Diagnosis of
Chronic Myocardial Infarction on Nonenhanced Cardiac Cine MRI. Radiology 2019, 291, 606–617. [CrossRef] - Attia, Z.I.; Kapa, S.; Lopez-Jimenez, F.; McKie, P.M.; Ladewig, D.J.; Satam, G.; Pellikka, P.A.; Enriquez-Sarano, M.; Noseworthy, P.A.;
Munger, T.M.; et al. Screening for Cardiac Contractile Dysfunction Using an Artificial Intelligence–Enabled Electrocardiogram.
Nat. Med. 2019, 25, 70–74. [CrossRef] [PubMed] - Bachtiger, P.; Petri, C.F.; Scott, F.E.; Ri Park, S.; Kelshiker, M.A.; Sahemey, H.K.; Dumea, B.; Alquero, R.; Padam, P.S.; Hatrick, I.R.;
et al. Point-of-Care Screening for Heart Failure with Reduced Ejection Fraction Using Artificial Intelligence during ECG-Enabled
Stethoscope Examination in London, UK: A Prospective, Observational, Multicentre Study. Lancet Digit. Health 2022, 4, e117–e125.
[CrossRef] [PubMed] - Yao, X.; Rushlow, D.R.; Inselman, J.W.; McCoy, R.G.; Thacher, T.D.; Behnken, E.M.; Bernard, M.E.; Rosas, S.L.; Akfaly, A.; Misra, A.;
et al. Artificial Intelligence–Enabled Electrocardiograms for Identification of Patients with Low Ejection Fraction: A Pragmatic,
Randomized Clinical Trial. Nat. Med. 2021, 27, 815–819. [CrossRef] [PubMed] - Duffy, G.; Cheng, P.P.; Yuan, N.; He, B.; Kwan, A.C.; Shun-Shin, M.J.; Alexander, K.M.; Ebinger, J.; Lungren, M.P.; Rader, F.; et al.
High-Throughput Precision Phenotyping of Left Ventricular Hypertrophy With Cardiovascular Deep Learning. JAMA Cardiol.
2022, 7, 386–395. [CrossRef] [PubMed] - Narula, S.; Shameer, K.; Salem Omar, A.M.; Dudley, J.T.; Sengupta, P.P. Machine-Learning Algorithms to Automate Morphological
and Functional Assessments in 2D Echocardiography. J. Am. Coll. Cardiol. 2016, 68, 2287–2295. [CrossRef] [PubMed] - Frazer, J.; Notin, P.; Dias, M.; Gomez, A.; Min, J.K.; Brock, K.; Gal, Y.; Marks, D.S. Disease Variant Prediction with Deep Generative
Models of Evolutionary Data. Nature 2021, 599, 91–95. [CrossRef] [PubMed] - Zhou, H.; Li, L.; Liu, Z.; Zhao, K.; Chen, X.; Lu, M.; Yin, G.; Song, L.; Zhao, S.; Zheng, H.; et al. Deep Learning Algorithm
to Improve Hypertrophic Cardiomyopathy Mutation Prediction Using Cardiac Cine Images. Eur. Radiol. 2020, 31, 3931–3940.
[CrossRef] [PubMed]
- Hathaway, J.; Heliö, K.; Saarinen, I.; Tallila, J.; Seppälä, E.H.; Tuupanen, S.; Turpeinen, H.; Kangas-Kontio, T.; Schleit, J.;
Tommiska, J.; et al. Diagnostic Yield of Genetic Testing in a Heterogeneous Cohort of 1376 HCM Patients. BMC Cardiovasc. Disord.
2021, 21, 126. [CrossRef] - Li, X.; Yang, L.; Yuan, Z.; Lou, J.; Fan, Y.; Shi, A.; Huang, J.; Zhao, M.; Wu, Y. Multi-Institutional Development and External
Validation of Machine Learning-Based Models to Predict Relapse Risk of Pancreatic Ductal Adenocarcinoma after Radical
Resection. J. Transl. Med. 2021, 19, 281. [CrossRef] - Kaissis, G.A.; Jungmann, F.; Ziegelmayer, S.; Lohöfer, F.K.; Harder, F.N.; Schlitter, A.M.; Muckenhuber, A.; Steiger, K.; Schirren, R.;
Friess, H.; et al. Multiparametric Modelling of Survival in Pancreatic Ductal Adenocarcinoma Using Clinical, Histomorphological,
Genetic and Image-Derived Parameters. J. Clin. Med. 2020, 9, 1250. [CrossRef] - Zhang, Y.; Zhu, S.; Yuan, Z.; Li, Q.; Ding, R.; Bao, X.; Zhen, T.; Fu, Z.; Fu, H.; Xing, K.; et al. Risk Factors and Socio-Economic
Burden in Pancreatic Ductal Adenocarcinoma Operation: A Machine Learning Based Analysis. BMC Cancer 2020, 20, 1161.
[CrossRef] [PubMed] - Pépin, J.-L.; Letesson, C.; Le-Dong, N.N.; Dedave, A.; Denison, S.; Cuthbert, V.; Martinot, J.-B.; Gozal, D. Assessment of
Mandibular Movement Monitoring With Machine Learning Analysis for the Diagnosis of Obstructive Sleep Apnea. JAMA Netw.
Open 2020, 3, e1919657. [CrossRef] [PubMed] - Zhou, C.-M.; Xue, Q.; Ye, H.-T.; Wang, Y.; Tong, J.; Ji, M.-H.; Yang, J.-J. Constructing a Prediction Model for Difficult Intubation of
Obese Patients Based on Machine Learning. J. Clin. Anesth. 2021, 72, 110278. [CrossRef] [PubMed] - Carron, M.; Safaee Fakhr, B.; Ieppariello, G.; Foletto, M. Perioperative Care of the Obese Patient. Br. J. Surg. 2020, 107, e39–e55.
[CrossRef] [PubMed] - Ermer, S.C.; Farney, R.J.; Johnson, K.B.; Orr, J.A.; Egan, T.D.; Brewer, L.M. An Automated Algorithm Incorporating Poincaré
Analysis Can Quantify the Severity of Opioid-Induced Ataxic Breathing. Anesth. Analg. 2020, 130, 1147–1156. [CrossRef] [PubMed] - Ingrande, J.; Gabriel, R.A.; McAuley, J.; Krasinska, K.; Chien, A.; Lemmens, H.J.M. The Performance of an Artificial Neural
Network Model in Predicting the Early Distribution Kinetics of Propofol in Morbidly Obese and Lean Subjects. Anesth. Analg.
2020, 131, 1500–1509. [CrossRef] [PubMed] - Yang, Z.; Zhang, M.; Li, C.; Meng, Z.; Li, Y.; Chen, Y.; Liu, L. Image Classification for Automobile Pipe Joints Surface Defect
Detection Using Wavelet Decomposition and Convolutional Neural Network. IEEE Access 2022, 10, 77191–77204. [CrossRef] - Bellini, V.; Guzzon, M.; Bigliardi, B.; Mordonini, M.; Filippelli, S.; Bignami, E. Artificial Intelligence: A New Tool in Operating
Room Management. Role of Machine Learning Models in Operating Room Optimization. J. Med. Syst. 2020, 44, 20. [CrossRef] - Rozario, N.; Rozario, D. Can Machine Learning Optimize the Efficiency of the Operating Room in the Era of COVID-19? Can. J.
Surg. 2020, 63, E527–E529. [CrossRef] - Brennan, M.; Puri, S.; Ozrazgat-Baslanti, T.; Feng, Z.; Ruppert, M.; Hashemighouchani, H.; Momcilovic, P.; Li, X.; Wang, D.Z.;
Bihorac, A. Comparing Clinical Judgment with the MySurgeryRisk Algorithm for Preoperative Risk Assessment: A Pilot Usability
Study. Surgery 2019, 165, 1035–1045. [CrossRef] - Xue, B.; Li, D.; Lu, C.; King, C.R.; Wildes, T.; Avidan, M.S.; Kannampallil, T.; Abraham, J. Use of Machine Learning to Develop
and Evaluate Models Using Preoperative and Intraoperative Data to Identify Risks of Postoperative Complications. JAMA Netw.
Open 2021, 4, e212240. [CrossRef] [PubMed] - Tavolara, T.E.; Gurcan, M.N.; Segal, S.; Niazi, M.K.K. Identification of Difficult to Intubate Patients from Frontal Face Images
Using an Ensemble of Deep Learning Models. Comput. Biol. Med. 2021, 136, 104737. [CrossRef] [PubMed] - Cheney, F.W. The American Society of Anesthesiologists Closed Claims Project. Anesthesiology 1999, 91, 552–556. [CrossRef]
[PubMed] - León, M.A.; Räsänen, J. Neural Network-Based Detection of Esophageal Intubation in Anesthetized Patients. J. Clin. Monit. 1996,
12, 165–169. [CrossRef] [PubMed] - Ahn, J.C.; Connell, A.; Simonetto, D.A.; Hughes, C.; Shah, V.H. Application of Artificial Intelligence for the Diagnosis and
Treatment of Liver Diseases. Hepatology 2021, 73, 2546–2563. [CrossRef] [PubMed] - Hashimoto, R.; Requa, J.; Dao, T.; Ninh, A.; Tran, E.; Mai, D.; Lugo, M.; El-Hage Chehade, N.; Chang, K.J.; Karnes, W.E.; et al.
Artificial Intelligence Using Convolutional Neural Networks for Real-Time Detection of Early Esophageal Neoplasia in Barrett’s
Esophagus (with Video). Gastrointest. Endosc. 2020, 91, 1264–1271.e1. [CrossRef] [PubMed] - Ebigbo, A.; Mendel, R.; Probst, A.; Manzeneder, J.; Prinz, F.; de Souza, L.A., Jr.; Papa, J.; Palm, C.; Messmann, H. Real-Time Use of
Artificial Intelligence in the Evaluation of Cancer in Barrett’s Oesophagus. Gut 2019, 69, 615–616. [CrossRef] - Kohli, A.; Holzwanger, E.A.; Levy, A.N. Emerging Use of Artificial Intelligence in Inflammatory Bowel Disease. World J.
Gastroenterol. 2020, 26, 6923–6928. [CrossRef] - Waljee, A.K.; Liu, B.; Sauder, K.; Zhu, J.; Govani, S.M.; Stidham, R.W.; Higgins, P.D.R. Predicting Corticosteroid-Free Biologic
Remission with Vedolizumab in Crohn’s Disease. Inflamm. Bowel Dis. 2018, 24, 1185–1192. [CrossRef] - Le Berre, C.; Sandborn, W.J.; Aridhi, S.; Devignes, M.-D.; Fournier, L.; Smaïl-Tabbone, M.; Danese, S.; Peyrin-Biroulet, L.
Application of Artificial Intelligence to Gastroenterology and Hepatology. Gastroenterology 2020, 158, 76–94.e2. [CrossRef] - Spann, A.; Yasodhara, A.; Kang, J.; Watt, K.; Wang, B.; Goldenberg, A.; Bhat, M. Applying Machine Learning in Liver Disease and
Transplantation: A Comprehensive Review. Hepatology 2020, 71, 1093–1105. [CrossRef] [PubMed]




